室温下,在pH=12的某溶液中,由水电离的c(OH-)为( )
A.1.0×10-7 mol/L
B.1.0×10-6 mol/L
C.1.0×10-4 mol/L
D.1.0×10-12 mol/L
通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | H-H | Cl-Cl | H-Cl |
| 生成1 mol化学键时 放出的能量(kJ/mol) | 436 | 243 | 431 |
则下列热化学方程式不正确的是( )
A. H2(g)+
H2(g)+ Cl2(g)===2HCl(g) ΔH=-91.5 kJ/mol
Cl2(g)===2HCl(g) ΔH=-91.5 kJ/mol
B.H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ/mol
C. H2(g)+
H2(g)+ Cl2(g)===HCl(g) ΔH=+91.5 kJ/mol
Cl2(g)===HCl(g) ΔH=+91.5 kJ/mol
D.2HCl(g)===H2(g)+Cl2(g) ΔH=+183 kJ/mol
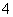 、Ba2+、Cl-、NO
、Ba2+、Cl-、NO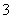
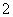 、Cl-、SO
、Cl-、SO
 、SO
、SO