0 142127 142135 142141 142145 142151 142153 142157 142163 142165 142171 142177 142181 142183 142187 142193 142195 142201 142205 142207 142211 142213 142217 142219 142221 142222 142223 142225 142226 142227 142229 142231 142235 142237 142241 142243 142247 142253 142255 142261 142265 142267 142271 142277 142283 142285 142291 142295 142297 142303 142307 142313 142321 203614
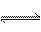 4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为( )
4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率v(X)(反应物的消耗速率或生成物的生成速率)可表示为( ) ClO+O2,ClO+O
ClO+O2,ClO+O

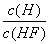 D.
D.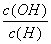
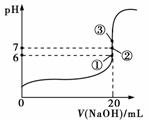
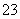 水解的缘故,请设计简单的实验事实证明之__________________。
水解的缘故,请设计简单的实验事实证明之__________________。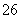 。
。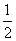 v(HI) ⑤c(HI):c(H2):c(I2)=2:1:1 ⑥温度和体积一定时,生成物浓度不再变化 ⑦温度和体积一定时,容器内的压强不再变化 ⑧条件一定时,混合气体的平均相对分子质量不再变化 ⑨温度和体积一定时,混合气体颜色不再变化 ⑩温度和压强一定时,混合气体的密度不再变化
v(HI) ⑤c(HI):c(H2):c(I2)=2:1:1 ⑥温度和体积一定时,生成物浓度不再变化 ⑦温度和体积一定时,容器内的压强不再变化 ⑧条件一定时,混合气体的平均相对分子质量不再变化 ⑨温度和体积一定时,混合气体颜色不再变化 ⑩温度和压强一定时,混合气体的密度不再变化