某兴趣小组对某溶液进行了多次的检测,其中三次检测结果如下表所示。请回答问题:
| 溶液中检测出的溶质 | |
| 第一次 | KCl、K2SO4 、Na2CO3、NaCl |
| 第二次 | KCl、K2CO3、Na2SO4、NaCl |
| 第三次 | KCl、BaCl2 、Na2CO3、NaCl |
(1)三次检测结果中,第 次的结果肯定不正确。
(2)该小组成员进行了如下实验,进一步确定溶液中存在SO42-、CO32-和Cl-,请将空格填充完整:
| 实验步骤 | 实验操作 | 实验目的 | 反应的离子方程式 |
| 第一步 | 向溶液中滴加过量的硝酸 | 检验 ① 的存在 | ② |
| 第二步 | 继续滴加过量的 ③ 溶液 | 检验SO42-的存在 | ④ |
| 第三步 | 过滤,再向滤液中滴加 ⑤ 溶液 | 检验 ⑥ 的存在 | Ag++Cl-=AgCl↓ |
(3)在上述实验的第一步中,不能将硝酸改为稀盐酸。原因是 。
观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
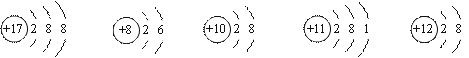 |
A B C D E
(1)属于离子结构示意图的是 (填字母编号)。
(2)性质最稳定的原子是 (填字母编号)。
(3)元素D的单质在B2中燃烧,该产物的化学式 。
(4)在核电荷数1-18的元素内,列举两个与C原子的电子层结构相同的离子,写出离子的符号 。
(5)写出化合物DAB在水溶液中的电离方程式 。
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是
| 30 mL盐酸 | 30 mL盐酸 | 30 mL盐酸 | |
| m(混合物) | 9.2 g | 15.7 g | 27.6 g |
| V(CO2)(标况) | 2.24 L | 3.36 L | 3.36 L |
A.向50 mL盐酸中加入混合物27.6 g时,盐酸过量
B.根据表中数据不能计算出混合物中NaHCO3的质量分数
C.15.7 g混合物与盐酸恰好能完全反应 D.盐酸的物质的量浓度为5.0 mol / L
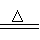 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O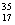 Cl
Cl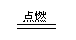 2FeCl3
2FeCl3