我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO4=FeSO4+Cu。有关该反应的说法正确的是
A.Fe被氧化 B.CuSO4是还原剂
C.Fe是氧化剂 D.CuSO4发生氧化反应
化学概念在逻辑上可能存在如下所示的关系,例如:纯净物与混合物属于并列关系。
 |
包含关系 并列关系 交叉关系
下列说法正确的是
A.氧化还原反应与化合反应属于交叉关系 B.电解质与化合物属于并列关系
C.单质与化合物属于包含关系 D.中和反应与复分解反应属于并列关系
Ⅰ.(1)现有pH相等、等体积的Ba(OH)2、NaOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合恰好中和, 则V1、V2、V3的大小关系是 ;
现有物质的量浓度相等、等体积的Ba(OH)2、NaOH和NH3·H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,混合后溶液呈中性,则V1、V2、V3的大小关系是 ;
(2)常温下,将浓度为amol/L的氨水与浓度为bmol/L的盐酸等体积混合,恰好呈中性(溶液体积变化忽略不计),则氨水的电离平衡常数Kb=
(3)氨水和NH4Cl等物质的量混合配制成的稀溶液,c(Cl-)<c(NH4+),下列说法错误的是( )
A、氨水的电离作用大于NH4Cl的水解作用 B、氨水的电离作用小于NH4Cl的水解作用
C、氨水的存在抑制了NH4Cl的水解 D、NH4Cl的存在抑制了氨水的电离
E、 c(H+)>c(OH-) F、 c(NH3•H2O)>c(NH4+)
G、c(NH3•H2O)+c(NH4+)=2c(Cl-) H、c(NH3•H2O)+c(OH-)=c(Cl-)+c(H+)
Ⅱ.某种甲酸酯水解反应方程式为:
HCOOR (l) + H2O(l) HCOOH (l) +ROH (l) △ H > 0
HCOOH (l) +ROH (l) △ H > 0
某小组通过实验研究该反应(反应过程中体积变化忽略不计)。反应体系中各组分的起始浓度如下表:
| 组分 | HCOOR | H2O | HCOOH | ROH |
| 物质的量浓度/mol·L一1 | 1.00 | 1. 99 | 0.01 | 0.52 |
甲酸酯转化率在温度T1下随反应时间(t)的变化如下图:.
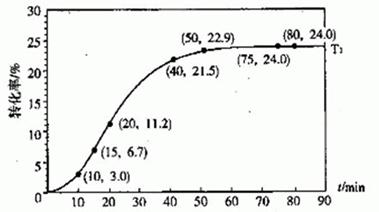
根据上述条件,计算不同时间范围内甲酸酯的平均反应速率,结果见下表:
| 反应时间/min | 0~5 | 10~15 | 20~25 | 30~35 | 40~45 | 50~55 | 75~80 |
| 平均速率/10-3mol·L-1·min-1 | 1.9 | 7.4 | 7.8 | 4.4 | 1.6 | 0.8 | 0.0 |
(1)T1温度下平衡体系中。c(ROH )为________ mol ·L一1
(2)15~20min范围内用甲酸酯表示的平均反应速率为________ mol ·L一1·min一1 ,(不要求写出计算过程)。
(3)根据题给数据分析,从影响反应速率的角度来看,生成物甲酸在该反应中还起到了_________的作用。

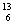 C呼气法在医学上常用于幽门螺旋杆菌的诊断,
C呼气法在医学上常用于幽门螺旋杆菌的诊断,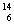 C可用来测定文物年代。下列有关
C可用来测定文物年代。下列有关
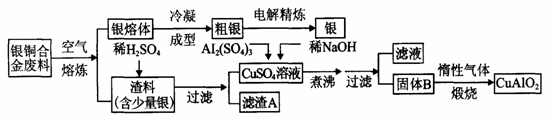
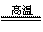 CuAlO2 + ↑
CuAlO2 + ↑