将碳棒和铁棒平行插入NaCl溶液,两棒的液面以上部分用铜丝相联并接入电流计,电流计指针偏转.以下说法正确的是( )
|
| A. | 电子自碳棒通过溶液流向铁棒 | B. | 电子自铁棒通过铜丝流向碳棒 |
|
| C. | 溶液中的H+得到电子放出H2 | D. | 铜丝失去电子发生氧化反应 |
下列实验可行的是( )
|
| A. | 用澄清石灰水检验CO中含有的CO2 |
|
| B. | 用BaCl2除去NaOH溶液中混有的少量Na2SO4 |
|
| C. | 用KSCN溶液检验溶液中含有的Fe2+ |
|
| D. | 用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
|
| A. | 溶液中导电粒子的数目减少 |
|
| B. | 溶液中 |
|
| C. | 醋酸的电离程度增大,c(H+)亦增大 |
|
| D. | 再加入10mLpH=11的NaOH溶液,混合液的pH=7 |
在密闭容器中进行如下反应:H2(g)+I2(g)⇌2HI(g);△H,在温度T1和T2时,产物的量与反应时间的关系如图所示.符合图示的正确判断是( )
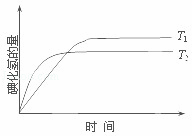
|
| A. | T1>T2,△H>0 | B. | T1>T2,△H<0 | C. | T1<T2,△H>0 | D. | T1<T2,△H<0 |
氯气是一种重要的工业原料.工业上利用反应在3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气.下列说法错误的是( )
|
| A. | 若管道漏气遇氨就会产生白烟 | B. | 该反应利用了Cl2的强氧化性 |
|
| C. | 该反应属于复分解反应 | D. | 生成1mol N2有6mol电子转移 |
用下列实验装置进行相应实验,能达到实验目的是( )
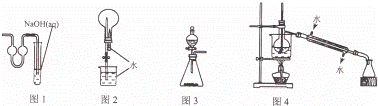
|
| A. | 用图1装置作为制取二氧化碳的尾气吸收装置 |
|
| B. | 用图2装置进行二氧化碳喷泉实验 |
|
| C. | 用图3装置进行二氧化锰和浓盐酸制取氯气的实验 |
|
| D. | 用图4装置进行石油的分馏实验 |
下列关于化学键的叙述正确的是( )
|
| A. | 非金属元素组成的化合物中只含共价键 |
|
| B. | C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键 |
|
| C. | 不同元素的原子构成的分子只含极性共价键 |
|
| D. | CH4中所有的价电子都参与形成共价键 |
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
|
| A. | 原子半径:Z>Y>X |
|
| B. | 气态氢化物的稳定性:R<W |
|
| C. | WX3和水反应形成的化合物是离子化合物 |
|
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3 主要:Cu2++CO32─+H2O═Cu(OH)2↓+CO2↑
次要:Cu2++CO32─═CuCO3↓
(2)CuSO4+Na2S 主要:Cu2++S2─═CuS↓
次要:Cu2++S2─+2H2O═Cu(OH)2↓+H2S↑
则下列几种物质的溶解度大小的比较中,正确的是( )
|
| A. | CuS<Cu(OH)2<CuCO3 | B. | CuS>Cu(OH)2>CuCO3 | C. | Cu(OH)2>CuCO3>CuS | D. | Cu(OH)2<CuCO3<CuS |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
|
| A. | 与铝反应产生大量氢气的溶液:Na+、K+、CO32﹣、NO3﹣ |
|
| B. | 甲基橙呈黄色的溶液:I﹣、Ba2+、AlO2﹣、Cl﹣ |
|
| C. | c(H+)=1.0×10﹣13mol/L溶液中C6H5O﹣、K+、SO42﹣、Br﹣ |
|
| D. | 1.0 mol•L﹣1的KNO3溶液:H+、Fe2+、Cl﹣、SO42﹣ |
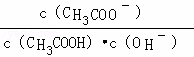 不变
不变