某溶液中含有大量的下列离子:Mg2+、NO3﹣、K+和M离子,经测定Mg2+、NO3﹣、K+离子的物质的量之比为2:4:1,则M离子可能是下列中的( )
|
| A. | Cl﹣ | B. | SO42﹣ | C. | OH﹣ | D. | Na+ |
为提纯下列物质(括号内物质为杂质),所选用的试剂和分离方法正确的是( )
| 物质 | 除杂试剂 | 分离方法 | |
| A | 硝酸铜溶液(硝酸银) | 铜粉 | 结晶 |
| B | NaCl溶液(CuCl2) | NaOH溶液 | 萃取 |
| C | 乙醇(水) | ________ | 分液 |
| D | 铜粉(铁粉) | 稀盐酸 | 过滤 |
|
| A. | A | B. | B | C. | C | D. | D |
在两个容积相同的容器中,一个盛有HCl气体,另一个盛有H2和CO2的混合气体.在同温同压下,两容器内的气体一定具有相同的( )
|
| A. | 原子数 | B. | 分子数 | C. | 质量 | D. | 密度 |
下列有关化学实验基本知识和基本操作的描述不正确的是( )
|
| A. | 丁达尔效应可以用于区别FeCl3溶液和Fe(OH)3胶体 |
|
| B. | 过滤和蒸发操作均用到玻璃棒,但玻璃棒的作用不相同 |
|
| C. | 加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32﹣ |
|
| D. | 先加入BaCl2溶液,再加入HNO3溶液,产生了白色沉淀,则溶液中一定含有大量的SO42﹣ |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
|
| A. | 常温常压下,32 g O2和O3的混合气体所含原子数为NA |
|
| B. | 标准状况下,1.8g的H2O中含有的电子数为NA |
|
| C. | 常温常压下,11.2L氧气所含的原子数为NA |
|
| D. | 10克氖气所含原子数约为6.02×1023 |
下列实验设计方案中,可行的是( )
|
| A. | 用洗气瓶中的NaOH溶液除去CO2中混有的HCl气体 |
|
| B. | 在某试样中加入NaOH溶液加热,产生能使蓝色石蕊试纸变红的气体即证明有NH4+ |
|
| C. | 焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察 |
|
| D. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
|
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、萃取、分液 |
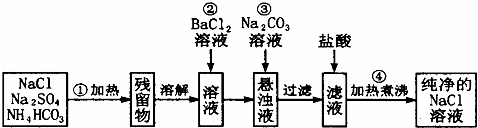
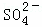 已除尽,方法是 取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42﹣已除尽 .
已除尽,方法是 取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42﹣已除尽 .