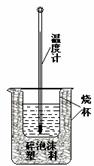
 实验室利用如右图装置进行中和热的测定。 回答下列问题:
实验室利用如右图装置进行中和热的测定。 回答下列问题:
⑴ 该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和_____________________。
⑵ 把温度为13℃,浓度为1.0mol·L-1的盐酸和1.1mol·L-1的碱溶液各50mL混合,
轻轻搅动,测得酸碱混合液的温度变化数据如下:
| 反应物 | 起始温度(℃) | 终了温度(℃) | 中和热(kJ·mol-1) |
| ①HCl+NaOH | 13 | 19.8 | -a |
| ②HCl+NH3·H2O | 13 | 19.3 | -b |
(Ⅰ) 则a_______b(填“>”、“<”、“=”)
(Ⅱ) 实验中碱液过量的目的是________________________________。
(Ⅲ) 已知:稀溶液的密度近似为1g/cm3,其比热容约为4.18J/(g.℃),则a = 。
己知A(g)+B(g) C(s)+2D(g)反应的平衡常数和温度的关系如下:
C(s)+2D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K= ,△H= 0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L﹣1•s﹣1,则6s时c(A)= mol•L﹣1。反应达到平衡时A的转化率为80%,如果这时向该密闭容器中再充入1mol氩气,达新平衡时A的转化率为 。
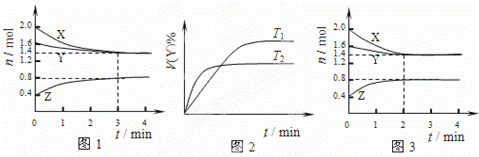
T℃时在2L容积不变的密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论错误的是( )
|
| A. | 容器中发生的反应可表示为:3X(g)+Y(g) |
|
| B. | 反应进行前3min内,用X表示的反应速率v(X)=0.1mol/(L•min) |
|
| C. | 若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
|
| D. | 保持其他条件不变,升高温度,化学平衡向逆反应方向移动 |
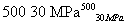 2NH3(g) ΔH=-38.6 kJ·mol-1
2NH3(g) ΔH=-38.6 kJ·mol-1 2Z(g)
2Z(g)