中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论正确的是( )。
| 选项 | 规律 | 结论 |
| A | 较强酸可以制取较弱酸 | 次氯酸溶液无法制取盐酸 |
| B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓、稀硝酸,浓硝酸中铝片先溶解完 |
| C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 | NH3沸点低于PH3 |
| D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加CuSO4溶液可以得到CuS沉淀 |
实验(1)50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。
①大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大”、“偏小”、“无影响”)。
②实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒 (填“能”、“不能”)。
③某同学用0.25mol/L的稀硫酸代替盐酸进行上述实验,实验数据如下表
i)请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温 度t2/℃ | 平均温度差 (t2-t1)/℃ | ||
| H2SO4溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
|
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
ii)近似认为0.55 mol/L NaOH溶液和0.25mol/L H2SO4溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热ΔH=______(保留小数点后一位)。
iii)上述实验结果的数值与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)____。
a.实验装置保温、隔热效果差 b.在量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有稀硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
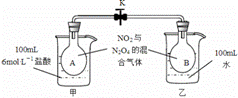 (2)如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲中盛放100ml、6 mol /L的HCl溶液,烧杯乙中盛放100ml水,(盐酸和水的起始温度相同)现向烧杯甲的溶液中加入25gNaOH固体,同时向烧杯乙中加入25gNH4NO3固体搅拌使之溶解:
(2)如图所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲中盛放100ml、6 mol /L的HCl溶液,烧杯乙中盛放100ml水,(盐酸和水的起始温度相同)现向烧杯甲的溶液中加入25gNaOH固体,同时向烧杯乙中加入25gNH4NO3固体搅拌使之溶解:
①A烧瓶中气体颜色 ,混合气体的平均分子量 (填“变大”、“变小”、“不变”)。
②B烧瓶中气体颜色 ,理由是 。

 CO2(g) ΔH=-437.3 kJ•mol-1
CO2(g) ΔH=-437.3 kJ•mol-1 CO(g) + H2(g)
CO(g) + H2(g) 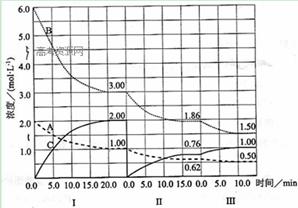 反应aA(g)+bB(g)
反应aA(g)+bB(g)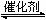 cC(g) (△H<0)在等 容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示:
cC(g) (△H<0)在等 容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如下图所示: CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2 和1 mol H2,在Ⅲ中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡时,下列说法正确的是( )
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 mol CO和1 mol H2O,在Ⅱ中充入1 mol CO2 和1 mol H2,在Ⅲ中充入2 mol CO 和2 mol H2O,700℃条件下开始反应。达到平衡时,下列说法正确的是( )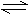 2HI(g)(正反应为放热反应)达到平衡后,下列说法不正确的是( )
2HI(g)(正反应为放热反应)达到平衡后,下列说法不正确的是( )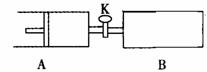 如图,关闭活塞K,向A中充入1 molX、1 molY,向B中充入2 molX、2 molY, 此时A的容积是a L,B的容积是2aL。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g)
如图,关闭活塞K,向A中充入1 molX、1 molY,向B中充入2 molX、2 molY, 此时A的容积是a L,B的容积是2aL。在相同温度和催化剂存在的条件下,使两容器中各自发生下述反应:X(g)+Y(g)  2Z(g)+W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L。下列说法错误的是( )
2Z(g)+W(g);△H<0。A保持恒压,B保持恒容,达平衡时,A的体积为1.4a L。下列说法错误的是( )