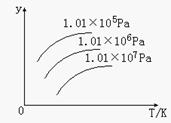
800℃时,在2L密闭容器中发生2NO(g)+O2(g)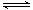 2NO2(g),测得n(NO)随时间的变化如下表:
2NO2(g),测得n(NO)随时间的变化如下表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)用O2表示2s时该反应的平均速率v =__________________。
(2)写出该反应的平衡常数表达式:K=__________________________ ___ 。已知:K(800℃)>K(850℃),该反应是__________(填“吸热”或“放热”)反应。
(3)能说明该反应已经达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.容器内气体的密度保持不变
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是_______。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂
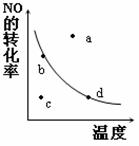
(5)下图中的曲线表示的是其他条件一定时,反应:2NO (g)+O2(g) 2NO2(g)中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 。
2NO2(g)中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是 。
A.a点 B.b点
C.c点 D.d点
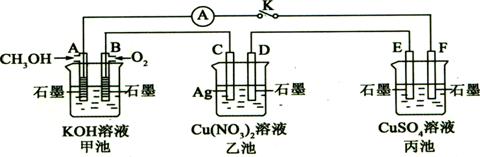
某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
 |
请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为 。
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为 。
(3)当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况)。
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母)。
A.Cu B.CuO C.Cu(OH)2 D.Cu2(OH)2CO3
 2NH3(g) △H1; CaCO3(s) == CaO(s)+CO2 (g) △H2
2NH3(g) △H1; CaCO3(s) == CaO(s)+CO2 (g) △H2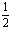 O2(g) == CO(g) △H1; C(s)+O2(g) == CO2(g) △H2
O2(g) == CO(g) △H1; C(s)+O2(g) == CO2(g) △H2 如图所示是298 K时,N2与H2反应过程中能量变化的曲线图,
如图所示是298 K时,N2与H2反应过程中能量变化的曲线图,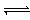 在密闭容器中进行下列反应:
在密闭容器中进行下列反应: 2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):
2CO(g) ΔH>0,起始通入2molCO,达到平衡后,改变下列条件,则指定物质的浓度、百分含量(填“不变”“增大”“减小”)及平衡如何变化(填“正移”“逆移”“不移动”):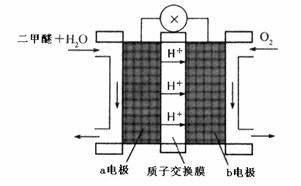
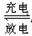 Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。
Ag2O+Zn+H2O在此电池放电时,正极的电极反应式为 。 2NO+O2,达到平衡的标志是( )
2NO+O2,达到平衡的标志是( ) 2NH3(g) △H<0
2NH3(g) △H<0