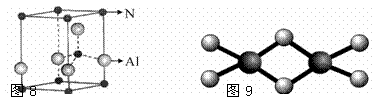
用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料,氮化铝(其晶胞如图8所示)可由氯化铝与氨经气相反应制得。
 |
(1)基态Cr的价电子排布式可表示为 ▲ 。
(2)氮化铝的化学式为 ▲ ,距离铝原子最近且距离相等的氮原子数目为 ▲ 个。
(3)氯化铝易升华,其双聚物Al2Cl6结构如图9所示。在Al2Cl6中存在的化学键有 ▲ (填字母)。
a.离子键 b.共价键 c.配位键 d.金属键
(4)一定条件下用Al2O3和CCl4反应制备AlCl3的反应为:Al2O3+3CCl4===2AlCl3+3COCl2。其中COCl2分子的空间构型为 ▲ 。一种与CCl4互为等电子体的分子的化学式为 ▲ 。
(5)AlCl3在下述反应中作催化剂。分子③中碳原子的杂化类型为 ▲ 。
 |
研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH 1=+489.0 kJ· mol-1,C(s) +CO2(g)=2CO(g) ΔH 2 =+172.5 kJ·mol-1, 则CO还原Fe2O3(s)的热化学方程式为 ▲ 。
 (2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 ▲ 。
(2)CO与O2设计成燃料电池(以KOH溶液为电解液)。该电池的负极反应式为 ▲ 。
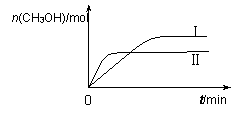
(3)CO2和H2充入一定体积的恒容密闭容器中,在两种温度下发生反应:CO2(g) +3H2(g) CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
CH3OH(g) +H2O(g) 测得CH3OH的物质的量随时间的变化如图5。
|
②一定温度下,在容积相同且固定的两个密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
| 容 器 | 甲 | 乙 |
| 反应物投入量 | 1molCO2、3molH2 | a molCO2、3a molH2、 b molCH3OH(g)、b molH2O(g) |
若甲中平衡后气体的压强为开始的0.8倍,要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为 ▲ 。
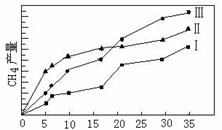
 (4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 ▲ (填序号)。
(4)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化如图6。在0~15小时内,CH4的平均生成速率I、II和III从小到大的顺序为 ▲ (填序号)。
|
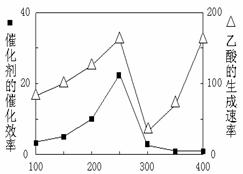
(5)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图7。
①当温度在 ▲ 范围时,温度是乙酸生成速率的主要影响因素。
②Cu2Al2O4可溶于稀硝酸,稀硝酸还原产物为NO,写出有关的离子方程式 ▲ 。
中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol•L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据计算PM2.5待测试样的pH = ▲ 。
(2)汽车发动机工作时会引发N2和O2反应,其能量变化示意图如图3:
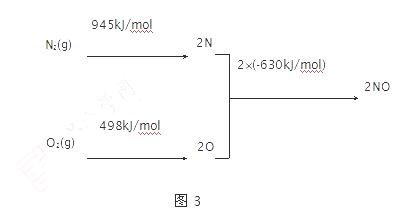
① N2(g)+O2(g) 2NO(g) ΔH= ▲ kJ·mol-1。
2NO(g) ΔH= ▲ kJ·mol-1。
② 尾气中空气不足时,NOx在催化转化器中被还原成N2。写出NO被CO还原的化学方程式 ▲ 。
③ 汽车汽油不完全燃烧时还产生CO,若设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g),已知该反应的ΔH>0,该设想能否实现? ▲ (填“能或不能”)。依据是 ▲ 。
碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如图4:
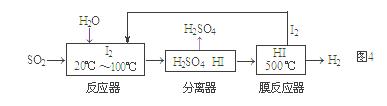
① 用离子方程式表示反应器中发生的反应 ▲ 。
② 用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是 ▲ 。
某化学兴趣小组对加碘食盐中的KIO3进行研究,它是一种白色粉末,常温下很稳定,加热至560 ℃开始分解。在酸性条件下KIO3是一种较强的氧化剂,与HI、H2O2等作用,被还原为碘单质。
(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取w g加碘盐,加适量蒸馏水溶解; b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3 mol·L-1的 Na2S2O3溶液滴定(滴定时的反应方程式:
I2+2S2O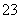 ===2I-+S4O
===2I-+S4O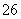 )。
)。
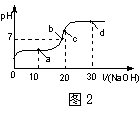
操作b涉及的主要反应的离子方程式为 ▲ ;滴定时,Na2S2O3溶液应放在 ▲ (填“酸式滴定管”或“碱式滴定管”),滴定至终点时消耗Na2S2O3溶液20.00 mL,其终点颜色变化为 ▲ ;加碘食盐样品中的碘元素含量是 ▲ mg·kg-1(以含w的代数式表示)。
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
| 顺序 | 步骤 | 实验现象 |
| ① | 取少量纯净的NaCl,加蒸馏水溶解 | 溶液无变化 |
| ② | 滴入淀粉KI溶液,振荡 | 溶液无变化 |
| ③ | 放置片刻,再滴加稀H2SO4,振荡 | 溶液变蓝色 |
请推测实验③中产生蓝色现象的可能原因是(用离子方程式表示): ▲ 。由学生乙的实验结果推知,学生甲的实验结果将 ▲ (填“偏大、偏小或无影响”)。
向2.0 L恒容密闭容器中充入1.0 mol PCl5,在温度为T℃时发生如下反应PCl5(g)  PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
PCl3(g)+C12(g) ΔH=+124 kJ·mol-1。反应过程中测定的部分数据见下表:
| 时间t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
回答下列问题: [已知:Ksp(Ag3 PO4) =1.4 × 10-16,Ksp(AgCl) =1.8 × 10-10]
(1)反应在前50 s的平均速率v(PCl5) = ▲ 。
(2)温度为T℃时,该反应的化学平衡常数= ▲ 。
(3)要提高上述反应的转化率,可采取的措施是 ▲ (任写一种)。
(4)在温度为T℃时,若起始时充入0.5 mol PCl5和a mol Cl2,平衡时PCl5的转化率仍为20%,则a= ▲ 。
(5)PCl5在热水中完全水解生成H3 PO4,该反应的化学方程式是 ▲ 。 若将0.01 mol PCl5投入l L热水中,再逐滴加入0.1 mol /L AgNO3溶液,先产生的沉淀是 ▲ 。
根据下列有关实验得出的结论一定正确的是
| 选项 | 操作 | 现象与结论 |
| A | 同温时,等质量的锌粒分别与足量稀硫酸反应 | 产生H2,氢气量:加胆矾=未加胆矾 |
| B | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液 | 溶液变黄,氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓 度的盐酸反应 | 粉状大理石产生气泡更快, 反应速率:粉状大理石>块状大理石 |
| D | 向浓度均为0.1 mol·L-1NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀, Ksp(AgCl)<Ksp(AgI) |