3,5—二甲氧基苯酚是重要的有机合成中间体,其合成反应如下:
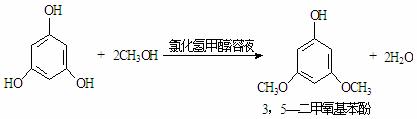
该反应后的混合物含有:3,5—二甲氧基苯酚、甲醇、水和HCl。
已知:甲醇、乙醚和3,5—二甲氧基苯酚的部分物理性质如下表:
| 物质 | 沸点/℃ | 熔点/℃ | 密度(20℃)/(g/cm3) | 溶解性 |
| 甲醇 | 64.7 | — | 0.7915 | 易溶于水 |
| 乙醚 | 34.5 | — | 0.7138 | 难溶于水 |
| 3,5—二甲氧基苯酚 | 172 | 36 | — | 易溶于甲醇、乙醚, 微溶于水 |
现在实验室对反应后的混合物进行分离提纯:
(1)利用与其它物质 差异较大的特点,可先用蒸馏法分离出甲醇,蒸馏操作时使用的玻璃仪器有:酒精灯、 、温度计、冷凝管 、接引管、锥形瓶。
(2)①蒸馏出甲醇后,加入乙醚进行 、 操作,有机层在分液漏斗的 层。
②双项选择:选用乙醚这种试剂的主要原因是( )
A.乙醚易挥发
B.3,5—二甲氧基苯酚在乙醚中溶解度大于在水中的溶解度
C.乙醚难溶于水
D.3,5—二甲氧基苯酚熔点较低
(3)经上述步骤分离得到的有机层再用饱和NaHCO3溶液洗涤,其目的是 。
(4)洗涤完成后,加入无水CaCl2干燥,过滤除去干燥剂,蒸馏除去乙醚,得到固体产物,为进一步提纯固体产物还要进行 操作。
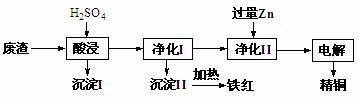
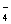 +10H+=5Fe3++Mn2++5H2O)
+10H+=5Fe3++Mn2++5H2O)

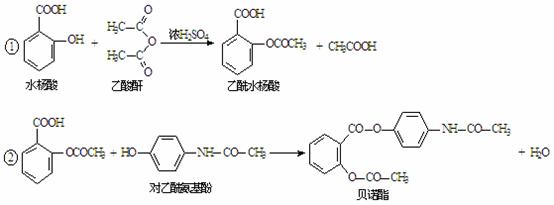
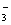 )+c(H+) = c(OH-)
)+c(H+) = c(OH-)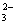 )
)