0 141647 141655 141661 141665 141671 141673 141677 141683 141685 141691 141697 141701 141703 141707 141713 141715 141721 141725 141727 141731 141733 141737 141739 141741 141742 141743 141745 141746 141747 141749 141751 141755 141757 141761 141763 141767 141773 141775 141781 141785 141787 141791 141797 141803 141805 141811 141815 141817 141823 141827 141833 141841 203614
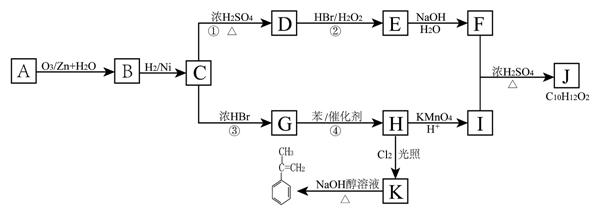
 (其中R、R1、R2、R3和R4均表示烃基)
(其中R、R1、R2、R3和R4均表示烃基) (4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。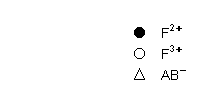 (5)化合物EF[F(AB)6]是一种蓝色晶体,右图表示其晶胞的
(5)化合物EF[F(AB)6]是一种蓝色晶体,右图表示其晶胞的 (E+未画出)。该蓝色晶体的一个晶胞中E+的个数为 。
(E+未画出)。该蓝色晶体的一个晶胞中E+的个数为 。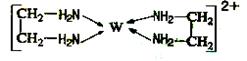
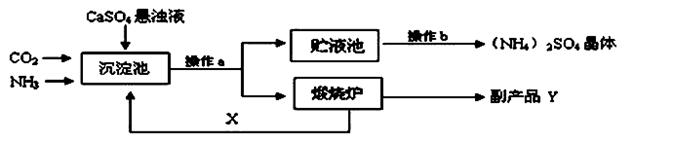
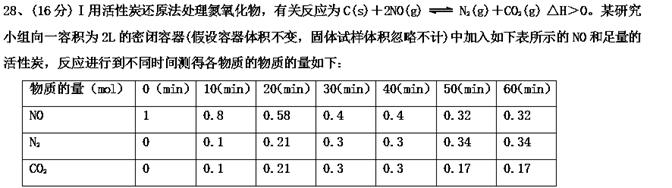 (1)10 min~20 min以v(CO2)表示的反应速率为________ mol·L-1·s-1。
(1)10 min~20 min以v(CO2)表示的反应速率为________ mol·L-1·s-1。
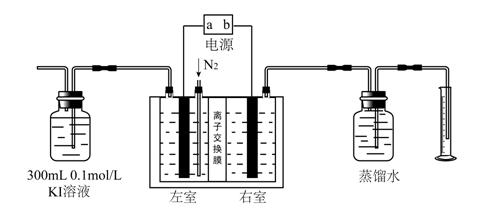
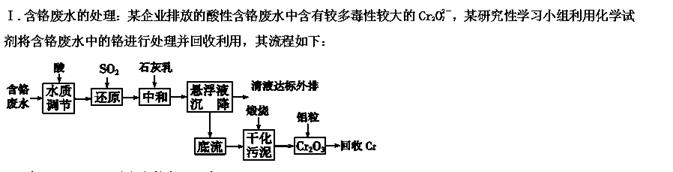 (1)请写出通入SO2时发生的离子反应:______________________________________。
(1)请写出通入SO2时发生的离子反应:______________________________________。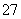 也可以使用其他还原剂,如电解还原法就是使用Fe电极电解酸性含铬废水,电解时产生的Fe2+作还原剂还原Cr2O
也可以使用其他还原剂,如电解还原法就是使用Fe电极电解酸性含铬废水,电解时产生的Fe2+作还原剂还原Cr2O Cr2O
Cr2O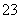 +
+