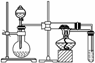某校化学研究性学习小组,在学习金属的冶炼以后,对一氧化碳还原金属氧化物的实验非常感兴趣,他们查阅有关资料后分析:
(1)学生对相关装置进行分析和比较发现这些装置既有各自的优点,同时也发现各个装置中均存在一些不足,具体看下表:
| 人教版、广东版、山东版 | 上海科学技术出版社 | 化学教学杂志 |
|
|
|
|
| 现象明显、有环保意识 | 现象明显、有环保意识且尾气得以利用 | 现象明显、有环保意识 |
| 不足之处:①反应结束滞留在装置中的一氧化碳无法处理;②进入硬质试管中的气体所含杂质没有处理;③经实验发现尾气点燃时有时燃烧有时不能燃烧,而且安全性差 |
(2)根据高三拓展教材中一氧化碳还原氧化铁的实验要求,在上述实验的基础上学生设计了相对更为合理的实验,重点避免了上述三个不足。其中一氧化碳的制备是利用甲酸和浓硫酸共热到60~80℃可发生脱水反应:
HCOOH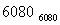 CO↑+H2O
CO↑+H2O
请根据以下各图进行选择形成一套相对较为合理的实验装置图(某些装置可重复使用)
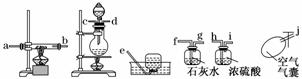
回答以下问题:
①合理实验装置的连接顺序是(写小写字母)________。
②在反应时强调先产生一氧化碳气体,一会再点燃加热氧化铁的酒精灯,原因是( )
A.因为一般反应从左到右进行
B.排除体系内的空气,使反应过程更安全
C.甲酸与浓硫酸反应可以产生大量的CO气体
D.此反应加热时间长有利于产生CO
③请说出你所选择的第一个石灰水洗气瓶的作用是_______________________
___________________________ _____________________________________________。
_____________________________________________。
④在观察到硬质玻璃管中由________色完全变为________色时停止加热,然后继续________,原因是防止铁被氧化。
⑤硬质玻璃管中发生反应的化学方程式是____________________________。
⑥该实验的一个优点是把实验过程中的尾气利用排水法收集起来,收集的气体前后有几瓶,若分别先后编号,点燃各个瓶中的气体,中间编号的集气瓶中气体________,前后编号的集体瓶中气体________,原因是____________________________________。
实验室以含有Ca2+、Mg2+、Cl-、SO 、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如
、Br-等离子的卤水为主要原料制备无水CaCl2和Br2,流程如 下:
下:
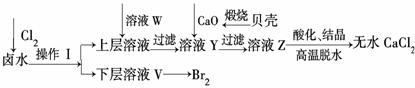
(1)操作Ⅰ使用的试剂是________,所用主要仪器的名称是________。
(2)加入溶液W的目的是________。用CaO调节溶液Y的pH,可以除去Mg2+。由表中数据可知,理论上可选择的pH最大范围是________。酸化溶液Z时,使用的试剂为________。
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8 mol·L-1 |
(3)实验室用贝壳与稀盐酸反应制备并收集CO2气体,下列装置中合理的是________。

(4)常温下,H2SO3的电离常数Kal=1.2×10-2,Ka2=6.3×10-3,H2CO3的电离常数Kal=4.5×10-7,Ka2=4.7×10-11。某同学设计实验验证H2SO3酸性强于H2CO3:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测两溶液的pH,若前者的pH小于后者,则H2SO3酸性强于H2CO3。该实验设计不正确,错误在于________。
设计合理实验验证H2SO3酸性强于H2CO3(简要说明实验步骤、现象和结论):________________________。仪器自选。
供选择的试剂:CO2、SO2、Na2CO3、NaHCO3、Na2SO3、NaHSO3、蒸馏水、饱和石灰水、酸性KMnO4溶液、品红溶液、pH试纸。
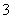 、Na+、SO
、Na+、SO 能大量共存
能大量共存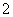 、NO
、NO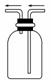 如图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )
如图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是 ( )