0 141263 141271 141277 141281 141287 141289 141293 141299 141301 141307 141313 141317 141319 141323 141329 141331 141337 141341 141343 141347 141349 141353 141355 141357 141358 141359 141361 141362 141363 141365 141367 141371 141373 141377 141379 141383 141389 141391 141397 141401 141403 141407 141413 141419 141421 141427 141431 141433 141439 141443 141449 141457 203614
 Cl、
Cl、 Cl为不同的核素,有不同的化学性质
Cl为不同的核素,有不同的化学性质
 ×
×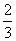 ×65 g·mol-1=78 g。
×65 g·mol-1=78 g。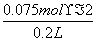 =0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。
=0.75 mol/L;②设合金中Na、K的物质的量分别为a mol、b mol,然后利用质量守恒与得失电子守恒可得方程式:a+b=0.75×2和23a+39b=5.05,解得a=0.050 mol、b=0.10 mol,故可得到合金的化学式为NaK2。 =
=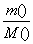 ,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。
,利用该式和题中数据可计算出三次实验中所取氢氧化钠样品的摩尔质量,进而可得出结论。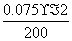 ×1 000=0.75 (mol/L)
×1 000=0.75 (mol/L)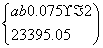
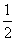 ×24=3 (mol)
×24=3 (mol)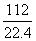 =5 (mol)
=5 (mol) ×2.40=40 (g/mol)
×2.40=40 (g/mol)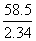 ×2.32=58 (g/mol)
×2.32=58 (g/mol) +H+===HCO
+H+===HCO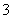 ,不生成CO2.C项,等质量的NaHCO3和Na2CO3分别与足量盐酸反应时,NaHCO3产生的CO2多.D项,向饱和Na2CO3溶液中通入CO2时发生反应:Na2CO3+CO2+H2O===2NaHCO3↓,反应中消耗H2O,且生成的NaHCO3溶解度小、质量多,故NaHCO3会结晶析出.
,不生成CO2.C项,等质量的NaHCO3和Na2CO3分别与足量盐酸反应时,NaHCO3产生的CO2多.D项,向饱和Na2CO3溶液中通入CO2时发生反应:Na2CO3+CO2+H2O===2NaHCO3↓,反应中消耗H2O,且生成的NaHCO3溶解度小、质量多,故NaHCO3会结晶析出.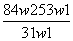 B.
B.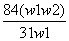
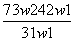 D.
D.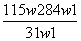
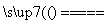 Na2CO3+CO2↑+H2O Δm
Na2CO3+CO2↑+H2O Δm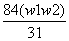 (g),
(g),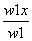 =
=