0 141181 141189 141195 141199 141205 141207 141211 141217 141219 141225 141231 141235 141237 141241 141247 141249 141255 141259 141261 141265 141267 141271 141273 141275 141276 141277 141279 141280 141281 141283 141285 141289 141291 141295 141297 141301 141307 141309 141315 141319 141321 141325 141331 141337 141339 141345 141349 141351 141357 141361 141367 141375 203614
 表示,下列关于这种微粒的叙述正确的是( )
表示,下列关于这种微粒的叙述正确的是( )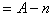 B. 所含中子数
B. 所含中子数
 D. 质量数
D. 质量数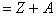
 与PH
与PH

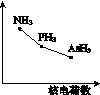

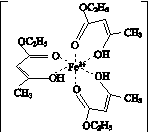
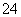 的立体构型为________。
的立体构型为________。