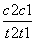草酸与高锰酸钾在酸性条件下能够发生如下反应:
MnO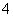 +H2C2O4+H+——Mn2++CO2↑+H2O(未配平)
+H2C2O4+H+——Mn2++CO2↑+H2O(未配平)
用4 mL 0.001 mol/L KMnO4溶液与2 mL 0.01 mol/L H2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
| Ⅰ | 2 | 20 | |
| Ⅱ | 2 | 20 | 10滴饱和MnSO4溶液 |
| Ⅲ | 2 | 30 | |
| Ⅳ | 1 | 20 | 1 mL蒸馏水 |
(1)该反应中氧化剂和还原剂的物质的量之比为________。
(2)如果研究催化剂对化学反应速率的影响,使用实验________和________(用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,使用实验________和________。
(3)对比实验Ⅰ和Ⅳ,可以研究________________________对化学反应速率的影响,实验Ⅳ中加入1 mL蒸馏水的目的是____________________________。
向体积为10 L的固定密闭容器中通入3 mol X气体,在一定温度下发生如下反应:
2X(g)  Y(g)+3Z(g)。
Y(g)+3Z(g)。
(1)经5 min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则用Y表示的反应速率为________mol/(L·min)。
(2)若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:
| 容器 | 反应速率 |
| 甲 | v(X)=3.5 mol/(L·min) |
| 乙 | v(Y)=2 mol/(L·min) |
| 丙 | v(Z)=4.5 mol/(L·min) |
| 丁 | v(X)=0.075 mol/(L·s) |
若其他条件相同,温度不同,则温度由高到低的顺序是(填序号)________________________。

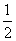 vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了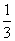 ,B的物质的量减少了
,B的物质的量减少了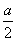 mol,有a mol D生成。
mol,有a mol D生成。 、y=________、p=________、q=________;
、y=________、p=________、q=________;
 ,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是: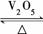 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )