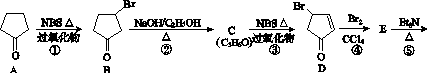席夫碱类化合物G在催化、药物、新材料等方面有广泛应用。合成G的一种路线如下:
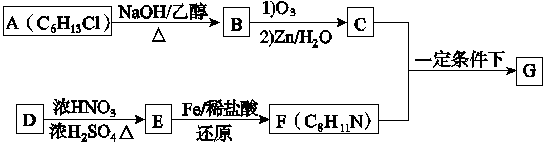
已知以下信息:
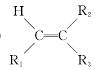 | |||
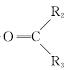 | |||
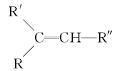
① 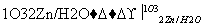 R1CHO+
R1CHO+
②1 mol B经上述反应可生成2 mol C,且C不能发生银镜反应
③D属于单取代芳烃,其相对分子质量为106
④核磁共振氢谱显示F苯环上有两种化学环境的氢
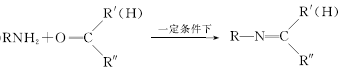 |
⑤ +H2O
回答下列问题:
(1)由A生成B的化学方程式为__________________,反应类型为________________。
(2)D的化学名称是________,由D生成E的化学方程式为________________________________________________________________________。
(3)G的结构简式为______________________________________________。
(4)F的同分异构体中含有苯环的还有________种(不考虑立体结构),其中核磁共振氢谱为4组峰,且面积比为6∶2∶2∶1的是____________(写出其中一种的结构简式)。
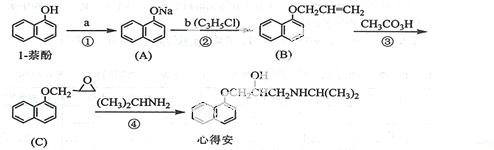
(5)由苯及化合物C经如下步骤可合成N异丙基苯胺。
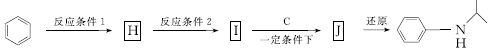 |
N异丙基苯胺
反应条件1所选用的试剂为________________,反应条件2所选用的试剂为______________,Ⅰ的结构简式为_________________________________________________。
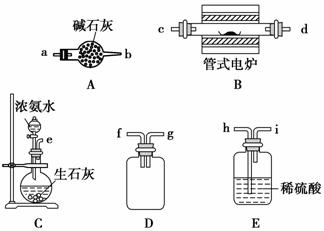
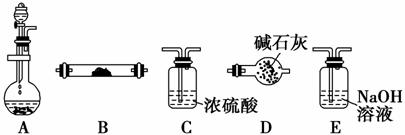
下列实验方案中,不能达到实验目的的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br在NaOH溶液中是否发生水解 | 将CH3CH2Br与NaOH溶液共热。冷却后,取出上层水溶液,用稀HNO3酸化,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色 |
| D | 验证Fe(OH)3的溶解度小于Mg(OH)2 | 将FeCl3溶液加入Mg(OH)2悬浊液中,振荡,可观察到沉淀由白色变为红褐色 |

 苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________。
苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液,能除去的副产物是________。

 (4)已知: +
(4)已知: + 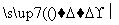 +H2O,则经反应路线②得到一种
+H2O,则经反应路线②得到一种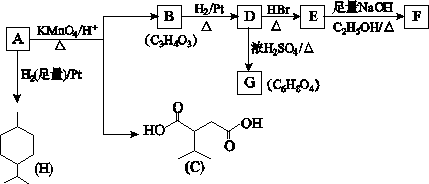
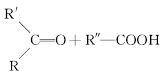
 已知:
已知: 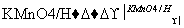
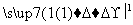 X
X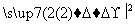 Y
Y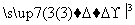 试剂b
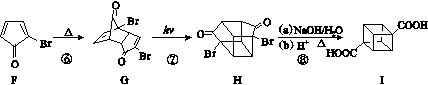
试剂b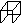 )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物Ⅰ的一种合成路线:
)具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点。下面是立方烷衍生物Ⅰ的一种合成路线: