(1)类比法是化学学习中常用的方法,已知硝酸能把铁氧化成Fe(NO3)3,但当铁过量时,产物是Fe(NO3)2。某同学受此启发,提出一个相似的观点:氯气与铁粉反应,当Cl2足量时生成FeCl3,当铁粉过量时产物是FeCl2,为了验证该观点是否正确,该同学将一定量的铁粉与Cl2恰好完全反应得到一固体物质,然后通过实验确定其成分。探究过程如下:
①提出假设:
假设1:该固体物质是FeCl2
假设2:该固体物质是FeCl3
 假设3:该固体物质是__________________。
假设3:该固体物质是__________________。
②设计实验方案:
取少量固体物质于烧杯中,加适量水溶解,得到溶液A,然后取两份A溶液分别进行实验,实验现象与结论如下表:
| 实验方法 | 实验现象 | 结 |
| 在溶液中加KSCN溶液 | 固体物质中有FeCl3 | |
| 在KMnO4溶液中加少量A溶液 | KMnO4溶液颜色无明显变化 | 固体物质中不含________ |
③根据上述实验结论,写出Cl2与铁粉加热时反应的化学方程式_________________。
(2)为了进一步探究FeCl3溶液的性质,该同学又利用A溶液作了如下一些实验,其中正确的是________。
A.将A溶液滴入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔现象
B.在A溶液中加入淀粉KI溶液,溶液变蓝
C.在A溶液中滴加NaOH浓溶液,出现红褐色沉淀
D.在A溶液中加入Fe、Cu固体后,充分反应后剩余固体中不可能有Fe无Cu
E.将A溶液加热蒸干并灼烧,得到FeCl3固体
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤: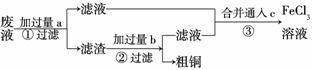
写出一个能证明还原性Fe比Cu强的 离子方程式:________
离子方程式:________ _______________________
_______________________
________________________________________________________________________。该反应在上图步骤
________中发生。请根据上述反应设计一个原电池,在方框中画出简易装置图(标出电极名称、电极材料、电解质溶液)。

上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及主要的电极反应式________________________________________________
_______________________________________________________ _________________。
_________________。
 ____Cu+____CuCl2+____N2↑+____H2O。
____Cu+____CuCl2+____N2↑+____H2O。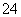 按氧化性由强到弱的顺序排列为____________。
按氧化性由强到弱的顺序排列为____________。 +C2O
+C2O 。下列有关叙述正确的是( )
。下列有关叙述正确的是( ) 化学反应中只能做氧化剂不能做还原剂
化学反应中只能做氧化剂不能做还原剂