Ⅰ.已知25℃时部分弱电解质的电离平衡常数数据如下表
| 化学式 | 电离常数(25 ℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | Ka1=4.3×10-7、K a2=5.6×10-11 |
| H2SO3 | Ka1=1.0×10-2、K a2=1.02×10-7 |
 (1)25 ℃时,物质的量浓度均为0.1mol•L-1的四种溶液:a.NaCN溶液 b.Na2CO3溶液c.CH3COONa溶液 d.NaHCO3溶液 , pH由大到小的顺序为________________________。(用字母表示)。
(1)25 ℃时,物质的量浓度均为0.1mol•L-1的四种溶液:a.NaCN溶液 b.Na2CO3溶液c.CH3COONa溶液 d.NaHCO3溶液 , pH由大到小的顺序为________________________。(用字母表示)。
(2)向NaCN溶液中通入少量的CO2,发生反应的离子方程式为_________________ _
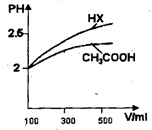
(3)体积均为100 mL、pH均为2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如上图所示,则HX的电离平衡常数_______(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
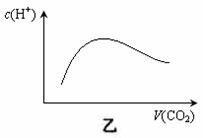
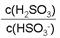 (4)25℃时,若向NaHSO3溶液中加入少量的I2,则溶液中 将_ ___ (填“增大”、“减小”或“不变”)
(4)25℃时,若向NaHSO3溶液中加入少量的I2,则溶液中 将_ ___ (填“增大”、“减小”或“不变”)
Ⅱ(5)过氧化尿素(CO(NH2)2·H2O2)是一种新型漂白、消毒剂,其活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品2.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL 6mol/LH2SO4,然后用0.1000mol/L KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液不与尿素反应),至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液6.000mL:
 完成并配平下列化学方程式:
完成并配平下列化学方程式:
MnO4— + H2O2 + H+ = Mn2+ + H2O +
② KMnO4溶液应盛放在 滴定管中,若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量 (填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量 (填“合格”或“不合格”),活性氧的质量分为 。
以下是一些物质的熔沸点数据(常压):
| 钾 | 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 63.65 | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 774 | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
金属钠和CO2在常压、890℃发生如下反应:
4 Na(g)+ 3CO2(g)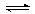 2 Na2CO3(l) + C(s,金刚石) △H=-1080.9kJ/mol
2 Na2CO3(l) + C(s,金刚石) △H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为 ;
若4v正(Na)= 3v逆(CO2),反应是否达到平衡 (选填“是”或“否”)。
(2)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
(3)NO2、O2和熔融NaNO3可制作燃料电池,其原理见图。该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应为:
若生成1molY,则需要消耗标准状况下氧气的体
积为 L。

 CH3OCH3(g)+CO2(g) △H<0。 如果上述反应方程式的平衡常数K值变大,则该反应_ (选填编号)。
CH3OCH3(g)+CO2(g) △H<0。 如果上述反应方程式的平衡常数K值变大,则该反应_ (选填编号)。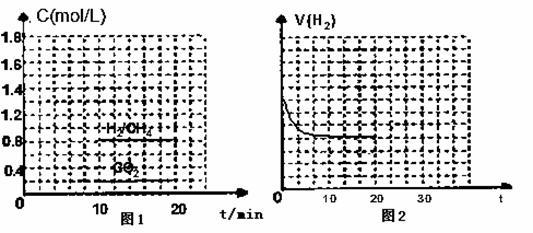
 (1)由石英砂可制取粗硅,其相关反应的热化学方程式为:
(1)由石英砂可制取粗硅,其相关反应的热化学方程式为: (2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g)
(2)粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:SiHCl3(g)+H2(g) Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;
Si(s)+3HCl(g)不同温度及不同n(H2)/n(SiHCl3)时,反应物X的平衡转化率关系如图;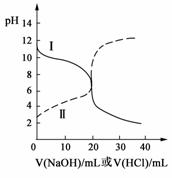 A.根据滴定曲线可得
A.根据滴定曲线可得
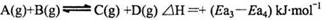
 CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大
CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大 xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是
xC(g) ΔH<0,平衡时M中A、B、C的物质的量之比为1∶3∶4。下列判断不正确的是