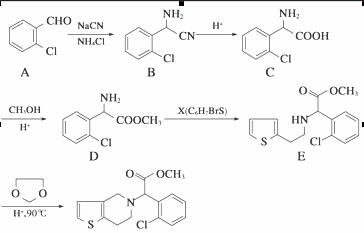
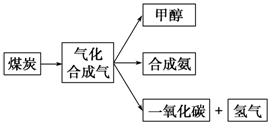
Ⅰ.下图是某煤化工产业链的一部分,试运用所学知识,解决下列问题:
(1)已知该产业链中某反应的平衡常数表达式为
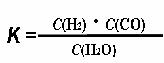 ,它所对应反应的化学方程式是 。
,它所对应反应的化学方程式是 。
(2)合成甲醇的主要反应是2H2(g)+CO(g)  CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
CH3OH(g) ΔH=-90.8 kJ·mol-1,t ℃下此反应的平衡常数为160。此温度下,在密闭容器中开始只加入CO、H2,反应10 min后测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度(mol·L-1) | 0.2 | 0.1 | 0.4 |
①该时间段内反应速率v(H2)=________。
②比较此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”)。
③反应达到平衡后,保持其它条件不变,若只把容器的体积缩小一半,平衡______(填“逆向”、“正向”或“不”)移动,平衡常数K____________(填“增大”、“减小”或“不变”)。
(3)固氮是科学家致力研究的重要课题。自然界中存在天然的大气固氮过程:
N2(g)+O2(g)===2NO(g) ΔH=+180.8 kJ·mol-1,工业合成氨则是人工固氮。
分析两种固氮反应的平衡常数,下列结论正确的是________________________________
(填字母序号)。
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2 000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
A.常温下,大气固氮和工业固氮都能非常容易进行
B.常温下,大气固氮与工业固氮完成程度相差不大
C.工业固氮时温度越低,氮气与氧气反应越完全
D.K越大说明合成氨反应的速率越大
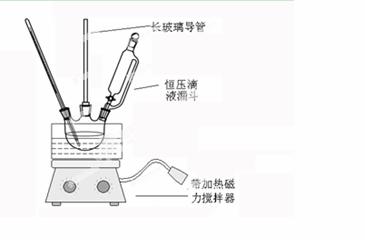
Ⅱ. 科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如下图所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO3固体,它在高温下能传导正极生成的O2-。
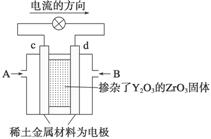
(1)c电极的名称为________。
(2)d电极上的电极反应式为 。
下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区的元素是 (填元素符号),价电子(外围电子)排布式为 。
(2)④ ⑤ ⑥ ⑦四种元素的第一电离能由大到小的顺序是 (用元素符号表示)。
(3)按原子轨道的重叠方式,③与⑥形成的化合物中,其中③的杂化方式为 ;
(4)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为 ;该元素与元素①形成的10电子分子X属于 分子(填“极性”或“非极性”)。
(5)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式: 。
(6)1183 K以下⑨元素形成的晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的原子间距离相同。
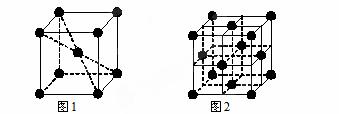
在1183 K以下的晶体中,与⑨原子等距离且最近的⑨原子数为______个,在1183 K以上的晶体中,与⑨原子等距离且最近的⑨原子数为________。