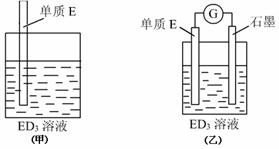
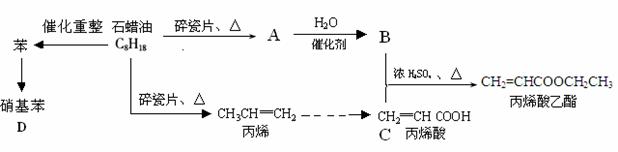
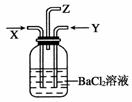
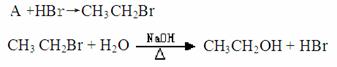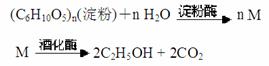某合作小组同学在进行酸性高锰酸钾溶液与草酸(化学式为H2C2O4,为弱酸,被氧化为CO2)溶液的反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。该小组通过实验探究其原因。
(1)该反应的离子方程式为
(2)该实验中反应速率明显加快的原因可能是
A.反应放热导致温度升高 B.反应物接触面积增大
C.生成物的催化作用 D.压强增大
(3)为验证该反应速率明显加快的原因,甲同学继续进行了下列实验,请完成下表。
| 编号 | 温度/℃ | 酸化的H2C2O4溶液/mL | KMnO4溶液/mL | 溶液褪色所需时间/s |
| 1 | 25 | 5.0 | 2.0 | 40 |
| 2 | 25 | (另加少量可溶于水的MnSO4粉末) |
| 4 |
| 3 | 60 |
|
| 25 |
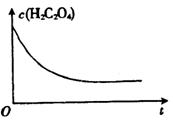
(4)已知25℃时,c(H2C2O4)~反应时间t的变化曲线如图,若保持其他条件不变,画出加入催化剂时c(H2C2O4)~反应时间t的变化曲线示意图(进行相应的标注)。
下表是元素周期表中短周期元素的一部分,表中所列字母分别代表一种元素。
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
(1)C的原子结构示意图为__________________
(2)A与G形成的化合物X的结构式为____________,其中X中含有的化学键是______ __,
X属于_________化合物(填“离子”或“共价”)。
(3)比较非金属性强弱G _____ H(填“>”或“<”)。
(4)在一定条件下,A与E可形成一种化合物Y,其相对分子质量与O2相同,则Y为___ ___; Y可在纯氧中燃烧,所得产物无污染,涉及的化学方程式为___________ __________
(5)“神舟”六号载人飞船内需要用化合物Z(由上表中的某2种元素组成)来吸收航天员呼出的CO2,请用化学方程式表示吸收原理___________ ________
(6)E的气态氢化物与其最高价氧化物水化物反应的产物W在一定温度下分解,生成两种氧化物,每1 mol W分解时转移的电子为4 mol ,W受热分解的化学方程式为_____ __
在一个容积固定的密闭容器中,发生反应:CO(g)+2H2(g) CH3OH(g) 正向为放热反应,第2 min时只改变一个条件,反应情况如下表:
CH3OH(g) 正向为放热反应,第2 min时只改变一个条件,反应情况如下表:
| 时间 | c(CO)/mol·L-1 | C(H2)/mol·L-1 | c(CH3OH)/mol·L-1 |
| 起始 | 1 | 3 | 0 |
| 第2 min | 0.8 | 2.6 | 0.2 |
| 第4 min | 0.4 | 1.8 | 0.6 |
| 第6 min | 0.4 | 1.8 | 0.6 |
下列说法不正确的是( )
A.第2 min时,如果只改变某一条件,则改变的条件可能是降低温度
B.第4 min至第6 min该化学反应处于平衡状态
C.第2 min时,如果只改变某一条件,则改变的条件可能是使用催化剂
D.第6 min时,其他条件不变,如果升高温度,正逆反应速率均增大

 D. 14C的原子结构示意图:
D. 14C的原子结构示意图:
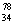 Se和
Se和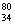 Se说法正确的是 ( )
Se说法正确的是 ( )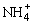 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下: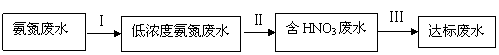

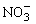 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下: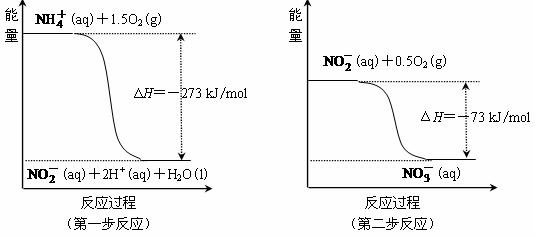
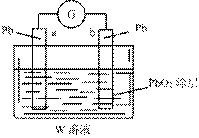
 +4H+=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g/cm3)变为_____ _mol/L。(计算结果保留两位小数)
+4H+=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g/cm3)变为_____ _mol/L。(计算结果保留两位小数)