铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(杂质中不含铁元素,且杂质不与H2、H2SO4反应)。某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究。
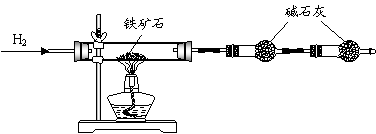 Ⅰ.铁矿石中含氧量的测定
Ⅰ.铁矿石中含氧量的测定
|
实验结果:将5.0g铁矿石放入硬质玻璃管中完全反应, 测得装置B增重1.35 g。
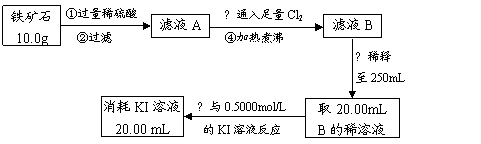 Ⅱ.铁矿石中含铁量的测定
Ⅱ.铁矿石中含铁量的测定
Ⅲ.问题讨论与解决:
(1)如要验证滤液A中铁元素的存在形式,可另取两份滤液A分别进行实验,实验方法、现象与结论如下表。请将其补充完整。
可供选择的试剂有:酸性KMnO4溶液、NaOH溶液、KSCN溶液、氯水
| 实验方法 | 实验现象 | 结论 |
| 步骤1:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe3+ |
| 步骤2:在滤液A中加入 ▲ | ▲ | 滤液A中有Fe2+ |
(2)步骤④中煮沸的作用是: ▲ ;
(3)步骤③中反应的离子方程式为: ▲ ;
(4)请通过实验Ⅰ、Ⅱ计算出该铁矿石中铁的氧化物的化学式。(写出计算过程)
某研究性学习小组为了测定某品牌合金中铝的含量,现设计了如下实验:
 |
已知:(1)该铝合金的主要成分为铝、镁、铜、硅。
(2)常温下,硅能和NaOH发生反应:Si+2NaOH+H2O===Na2SiO3+2H2↑。
请回答下列问题:
(1)固体A的成分是 ▲ ;
(2)生成固体B的离子方程式为 ▲ ;
步骤③中生成沉淀的离子方程式为 ▲ ;
(3)检验步骤③中沉淀是否洗涤干净的实验操作为 ▲
;
(4)该样品中铝的质量分数是 ▲ ;(用a、b表示)
(5)下列因操作不当,会使测定结果偏大的是 ▲ ;
A.第①步中加入NaOH溶液不足 B.第②步中加入盐酸不足时
C.第③步中沉淀未用蒸馏水洗涤 D.第④步对沉淀灼烧不充分
化学小组同学依据化学反应Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。
ZnSO4+SO2↑+2H2O制取22.4 L(标准状况)SO2气体。取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g·cm-3)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有氢气。为此,化学小组的同学设计了如下实验装置,对所制取的气体进行探究。

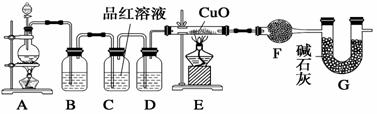
请回答下列问题:
(1)装置A中添加液体的仪器名称为 ▲ ;98%的浓H2SO4(ρ=1.84 g/cm3)的物质的量浓度是 ▲ ;
(2)请写出产生氢气的反应的离子方程式 ▲ ;
(3)①装置B是为了吸收SO2,则不能选用下列试剂中的 ▲ (填序号);
A.NaOH溶液 B.浓H2SO4 C.KMnO4溶液
②可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有氢气的实验现象是 ▲ ;
 2NO2中通入18O组成的氧气,重新达到平衡后,则18O
2NO2中通入18O组成的氧气,重新达到平衡后,则18O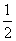 O2(g)=H2O(g);△H= a kJ/mol
O2(g)=H2O(g);△H= a kJ/mol  下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略)
下图表示各物质之间的转化关系。已知:常温下B、D、F、G、I、J是气体, F、G是空气中的主要成分,D是一种碱性气体。A中阴、阳离子个数比是1∶1, E是一种黑色氧化物,H是紫红色金属单质。(部分生成物和反应条件省略) 5NaCl+NaClO3+3H2O,以下叙述正确的
5NaCl+NaClO3+3H2O,以下叙述正确的 是
是