CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4 L容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2 (g)+CH4(g)
(g)+CH4(g) 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物质 | CH4 | CO2 | CO | H2 |
| 体积分数 | 0.1 | 0.1 | 0.4 |
|
①此温度下该反应的平衡常数K= 。
②已知:I.CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1
II.CO(g)+H2O (g)=CO2(g)+H2 (g) △H2 
III.2CO(g)+O2(g)=2CO2(g) △H3
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H= (用△H1 △H2 △H3表示)。
2CO(g)+2H2(g) 的△H= (用△H1 △H2 △H3表示)。
③对上述反应II:CO(g) + H2O(g)  CO2 (g)+ H2(g) ΔH 2 = −41 kJ/mol,起始时在密闭容器中充入1.00 molCO 和 1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副 反应的影响)。实验条件如下表:
CO2 (g)+ H2(g) ΔH 2 = −41 kJ/mol,起始时在密闭容器中充入1.00 molCO 和 1.00 molH2O,分别进行以下实验,探究影响平衡的因素(其它条件相同且不考虑任何副 反应的影响)。实验条件如下表:
①实验中c(CO2)随时间变化的关系见下图,请在答题卡的框图中,分别画 出实验②和③中c(CO2)随时间变化关系的预期结果示意图。
出实验②和③中c(CO2)随时间变化关系的预期结果示意图。

 (2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生 成速率如右图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
成速率如右图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因是 。
②为了提高该反应中CH4的转化率,可以采取的措施是 。
 (3)以甲醇为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,右图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
(3)以甲醇为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,右图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
①B极的电极反应式为 。
②若用该燃料电池做电源,用石墨做电极电解硫酸铜溶液,当电路中转移1mole— 时,实际上消耗的甲醇的质量比理论上大,可能原因是 。

 (4)沉锰工序中,298K、c(Mn2+)为1.05 mol•L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如右图所示。根据图中信息得出的结论是 。
(4)沉锰工序中,298K、c(Mn2+)为1.05 mol•L-1时,实验测得MnCO3的产率与溶液pH、反应时间的关系如右图所示。根据图中信息得出的结论是 。 (DMC)是一种新型的绿色有机合成中间体,其在生产中具有使用安全、方便、污染少、容易运输等特点。已知一定条件下,碳酸二甲酯能发生如下反应:
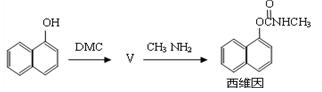
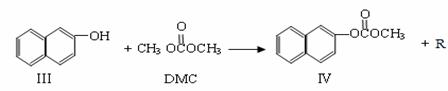
(DMC)是一种新型的绿色有机合成中间体,其在生产中具有使用安全、方便、污染少、容易运输等特点。已知一定条件下,碳酸二甲酯能发生如下反应: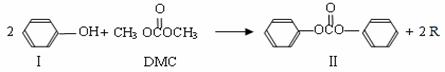
 DMC与足量NaOH溶液反应的化学方程式 。
DMC与足量NaOH溶液反应的化学方程式 。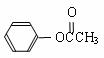 )在催化剂作用下也能生成化合物Ⅱ,同时得到一种副产品G,下列有关G的说法正确的是 。
)在催化剂作用下也能生成化合物Ⅱ,同时得到一种副产品G,下列有关G的说法正确的是 。 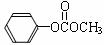 ),H的同分异构体有多种,请写出符合下列条件的H的一种同分异构体 。
),H的同分异构体有多种,请写出符合下列条件的H的一种同分异构体 。