|
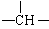 CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是 A.苹果酸中能发生酯化反应的官能团有2种
B.1mol苹果酸可与3mol NaOH发生中和反应
C.1mol苹果酸与足量金属Na反应生成生成1mol H2
D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
|
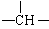 CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是 A.苹果酸中能发生酯化反应的官能团有2种
B.1mol苹果酸可与3mol NaOH发生中和反应
C.1mol苹果酸与足量金属Na反应生成生成1mol H2
D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体