某金属晶体M有两种堆积形式,如下图甲和乙,在T℃以上时甲可以转变为乙,这两种结构中最邻近的原子间距离相同。

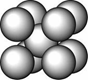
甲 乙
(1)乙的堆积方式称为 堆积;
甲和乙两种堆积方式中配位数之比为 ,晶胞边长之比为 。
(2)在T℃以下测定该金属晶体有关性质参数如下表所示。已知原子化热指1mol金属由固态转变为气态原子时所需要吸收的热量,是衡量金属键强弱的物理量。
| 金属 | 相对原子质量 | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22. 99 | 0. 960 | 108. 4 |
| M | 60. 20 | 7. 407 | 7735 |
预测该金属的熔点比Na (填“高”或“低”),由上述数据可计算M原子的原子半径为 pm。
(已知 ,7. 407≈
,7. 407≈ ,1pm=10
,1pm=10 m)
m)
已知A、B、C、D、E为短周期主族元素,它们的原子序数依次增大。请回答下列问题。
| A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 原子的第一至第四电离能分别是: I1=738kJ/mol I2 = 1451 kJ/mol I3 = 7733kJ/mol I4 = 10540kJ/mol |
| D | 元素的主族序数与周期数的差为3 |
| E | 元素是该周期电负性最大的元素 |
(1)B基态原子中能量最高的电子,其电子云在空间有 个伸展方向,原子轨道呈 形。B与A能形成多种形式的化合物,其中BA5属于离子晶体,其电子式为 。
(2)C的单质在一种常见的非金属氧化物中剧烈燃烧生成黑、白两种固体,写出该反应的化学方程式 ;其中的白色固体可用作耐火材料,它属于 晶体。
(3)BE3 在常温下是一种淡黄色的液体,构成其晶体的微粒之间的作用力是 ,它遇水即发生水解可生成一种具有漂白性的物质,写出反应的化学方程式 ,该反应说明其中B和E中非金属性较强的是 (填元素的符号)。
(4)DO2气体通入足量Ba(BO3)2的溶液,生成白色沉淀和无色气体,有关反应的离子方程式为 。
 (2)含铬废水有毒,危害很大.处理方法是在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.用离子方程式表示溶液pH不能超过10的原因 。
(2)含铬废水有毒,危害很大.处理方法是在含+6价铬的废水中加入一定量的硫酸和硫酸亚铁,使+6价铬还原成+3价铬;再调节溶液pH在6~8之间,使Fe3+和Cr3+转化为Fe(OH)3、Cr(OH)3沉淀而除去.用离子方程式表示溶液pH不能超过10的原因 。 (3)废水中的氨可以回收再利用。
(3)废水中的氨可以回收再利用。 2NH3(g)ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
2NH3(g)ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( ) 。
。