[选修3——物质结构与性质](15分)
I.下列化合物中,含有非极性共价键的离子化合物是
A.CaC2 B.N2H4 C.Na2S2 D.NH4NO3
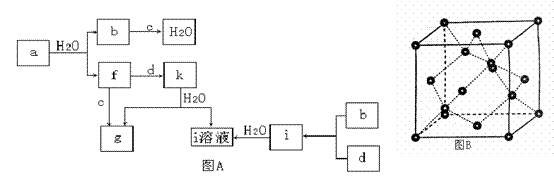
II. 图A所示的转化关系中(具体反应条件略),a、b、c和d分别为四种短周期元素的常见单质,其余均为它们的化合物,i的溶液为常见的酸,a的一种同素异形体的晶胞如图B所示。
 |
回答下列问题:
(1)图B对应的物质名称是 ,其晶胞中的原子数为 ,晶体类型为 。
(2)d中元素的原子核外电子排布式为 。
(3)图A中由二种元素组成的物质中,沸点最高的是 ,原因是 ,该物质的分子构型为 ,中心原子的杂化轨道类型为 。
(4)图A中的双原子分子中,极性最大的分子是 。
(5)k的分子式为 ,中心原子的杂化轨道类型为 ,属于 分子(填“极性”或“非极性”)。



 CO2 (g)+ H2 (g) , 已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 。
CO2 (g)+ H2 (g) , 已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于 。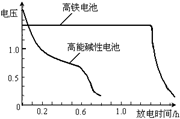
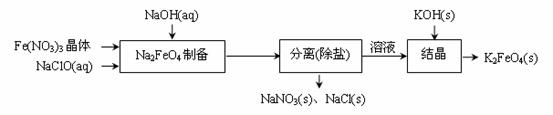
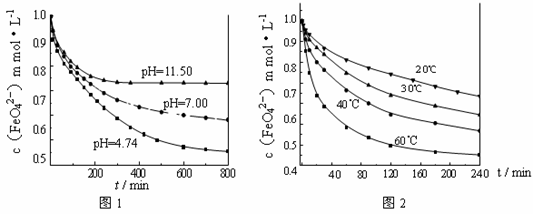
 4 Fe(OH)3 +8OH—+3 O2↑。 由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是
4 Fe(OH)3 +8OH—+3 O2↑。 由图1可知,800 min时,pH=11.50的溶液中高铁酸钾最终浓度比pH=4.74的溶液中高,主要原因是 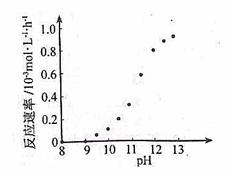 (1)电镀时,镀件与电源的 极连接。电镀铜时,电解质溶液应选用 (填化学式)。
(1)电镀时,镀件与电源的 极连接。电镀铜时,电解质溶液应选用 (填化学式)。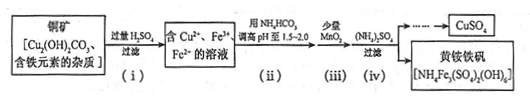
 某研究性学习小组设计实验探究铜与浓硫酸的反应。
某研究性学习小组设计实验探究铜与浓硫酸的反应。