已知X、Y是短周期主族元素,I为电离能,单位是可kJ/mol。根据下表所列数据判断不正确的是
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A.元素X的常见化合价是+1价 B.元素X与氯形成化合物时,化学式可能是XCl
C.元素Y是ⅢA族的元素 D.若元素Y处于第3周期,它可与冷水剧烈反应
下图是氮元素的几种价态与物质类别的对应关系:
 |
回答下列问题:
(1)写出N2的一种用途 。
(2)HNO3与上图中的物质C常用于检验Cl-的存在,则C的化学式为________。
(3)实验室制取物质B的化学方程式为 。
(4)NO2与水反应生成物质A的化学方程式为 。
(5)硝酸是一种强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2,稀硝酸的还原产物主要为NO。 实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(ⅰ) 请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:___________ _
_ 。
该反应中发生氧化反应的物质是__________,1 mol氧化剂_________(填“得到” 或“失去”)_______ mol电子。
(ⅱ) 48.0 g Cu与适量的浓HNO3反应,铜全部溶解后,共收集到标准状况下22.4 L的气体(NO2和NO的混合气体),反应中消耗HNO3的物质的量是( )
A.1.5 mol B.2.0 mol C.2.5 mol D.3.0 mol
(ⅲ) 实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、
N2、NH4NO3等。请将3种物质: FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对
应的横线上,组成一个未配平的化学方程式。
HNO3 + ______  ______ + ______ + N2O↑ + H2O
______ + ______ + N2O↑ + H2O
并配平其对应的离子方程式:□Fe2++□NO3-+□H+ =□Fe3++□N2O↑+□H2O
(ⅳ) 硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社
会提出的一个新概念——“绿色化学”,它要求从经济、环保和技术上设计可行的
化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是( )
A.Cu 
 Cu(NO3)2
Cu(NO3)2
B.Cu 
 CuO
CuO
 Cu(NO3)2
Cu(NO3)2
C.Cu 
 CuO
CuO
 Cu(OH)2
Cu(OH)2 
 Cu(NO3)2
Cu(NO3)2
D.Cu
 CuSO4
CuSO4 
 Cu(NO3)2
Cu(NO3)2
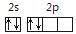 B.硫原子结构示意图:
B.硫原子结构示意图:


 Fe2(SO4)3+6H2O↑+3SO2↑和
Fe2(SO4)3+6H2O↑+3SO2↑和