下表为周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)⑩属于 区的元素,在该元素形成的二价离子的溶液中滴加氨水至过量,写出此过程中所有反应的离子方程式: 、
(2)写出元素⑨的基态原子的外围电子排布式
(3)写出与③同主族,其单质用来做半导体的元素符号 、
(4)下表列出了①、④元素形成的化学键的键能:
| 化学键 | ①—① | ①—④ | ④—④ | ④=④ | ④≡④ |
| 键能/kJ·mol−1 | 436.0 | 390.8 | 193 | 418 | 946 |
试写出①、④两单质发生反应的热化学方程式: ,
生成物的VSEPR模型是 ,空间构型为 ,键角为
(5)⑥ 、⑦ 两元素的最高价氧化物对应水化物的酸性最强的化学式是:
在一定体积的密闭容器中,进行如下化学反应: CO2(g)+H2(g ) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表:
| T/°C | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为________反应(填“吸热”“放热”)。
(2)能判断该反应是否已达化学平衡状态的依据是________。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.混合气体的平均密度不变
(3)某温度下,在2 L的密闭容器中,加入1 mol CO2和1 mol H2充分反应达平衡时,CO的平衡浓度为0.25 mol·L-1,试判断此时的温度为________℃。
(4)若在(3)所处的温度下,在1 L的密闭容器中,加入2 mol CO2和3 mol H2充分反应达平衡时,H2的物质的量为________。
a.等于1.0 mol b.大于1.0 mol c.大于0.5 mol d.无法确定
已知某化学反应的平衡常数表达式为 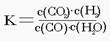 , 在不同的温度下该反应的平
, 在不同的温度下该反应的平
衡常数如下表:
| t ℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
下列有关叙述不正确的是( )
A.该反应的化学方程式是CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.若在1 L的密闭容器中通入CO2和H2各1 mol,5 min后温度升高到830 ℃,此时测得CO2为0.4 mol,该反应达到平衡状态
D.若平衡浓度符合关系式 ,则此时的温度为1 000 ℃
,则此时的温度为1 000 ℃



 PCl5(g) 测得平衡混合气PCl5为0.40mol;如果此时移走1.0mol PCl3和0.50mol Cl2,在温度不变时,重新达衡时PCl5的物质的量是( )
PCl5(g) 测得平衡混合气PCl5为0.40mol;如果此时移走1.0mol PCl3和0.50mol Cl2,在温度不变时,重新达衡时PCl5的物质的量是( ) 2C(g)+xD(g),经过10s达到平衡时,生成了2 mol C,经测定D的浓度为0.5 mol·L-1,下列判断正确的是( )
2C(g)+xD(g),经过10s达到平衡时,生成了2 mol C,经测定D的浓度为0.5 mol·L-1,下列判断正确的是( )