常温下,将FeCl3溶液和KI溶液混合,发生如下反应:
2Fe3++2I— 2Fe2++I2
2Fe2++I2
某研究小组为了证明FeCl3溶液和KI溶液的反应存在一定限度,设计了如下实验:取5 mL 0.1 mol·L—1 KI溶液,滴加0.1 mol·L—1 FeCl3溶液5~6滴,充分反应后溶液呈黄褐色,加入2 mL CCl4溶液,振荡后静置,取上层溶液,滴加KSCN试剂,观察实验现象。
已知:v(正)=k·cm(I—)·cn(Fe3+)(k为常数)
根据以上信息回答下列问题:
(1)能够证明反应存在限度的现象是1 。加入四氯化碳的作用是 。
(2)甲同学按上述步骤进行实验,结果并未观察到预期现象,推测可能原因是反应后溶液中Fe3+浓度过低。为此,甲又做了下列对比实验,实验结果记录如下:
| 氯化铁溶液用量 | 10滴 | 20滴 | 30滴 | 2 mL | 3 mL | 4 mL |
| 萃取后上层溶液颜色 | 黄色 | 黄色 | 黄色 | 较深黄色 | 黄色略带红色 | 黄红色 |
| 加入KSCN溶液后颜色 | 不变红 | 不变红 | 略变红 | 偏血红色 | 血红色 | 血红色 |
分析实验记录,甲认为导致Fe3+浓度过低的原因是 ;乙同学结合平衡移动的知识,认为还有一个原因是 。
(3)该反应的平衡常数表达式为 。
(4)已知改变I—、Fe3+的浓度,正反应速率对应数值如下表所示:
| c(I—)/mol·L—1 | c(Fe3+)/mol·L—1 | v/mol·L—1·s—1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
分析表中数据,I—浓度对反应速率的影响2 Fe3+浓度对反应速率的影响(填“大于”、“小于”或“等于”),理由是(写出计算过程)
。
(5)现将反应2Fe3++2I— 2Fe2++I2设计成下图所示的原电池
2Fe2++I2设计成下图所示的原电池

①能说明反应达到平衡的标志是 (填序号)。
a.电流计读数为零 b.电流计指针不再偏转且不为零
c.电流计指针偏转角度最大 d.甲烧杯中溶液颜色不再改变
②反应达平衡后,向甲中加入适量FeCl2固体,此时 (填“甲"或“乙”)中石墨电极为负极,对应的电极反应方程式为 。




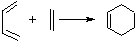

 和
和 为原料合成
为原料合成 ,请设计合成路线(注明反应条件)。
,请设计合成路线(注明反应条件)。 注:合成路线流程图示例如下:
注:合成路线流程图示例如下:

