800℃时,在2L密闭容器内,发生反应:2NO(g)+O2(g) 2NO2(g),已知在此体系中,n(NO)随时间的变化如表:
2NO2(g),已知在此体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)已知升高温度,NO2的浓度减小,则该反应是 (填“吸”或“放”)热反应。
(2)该反应平衡常数K的表达式为 。
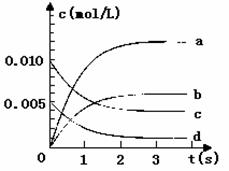
(3)右图中表示NO2的变化的曲线是 。
用O2表示从0~2 s内该反应的平均速率v= 。
(4)为使该反应的反应速率增大,且平衡向正反应
方向移动的是 。
a.及时分离除NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
氮是一种地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义。
(1)下图是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,写出NO2和CO反应的热化学方程式 ___________________ 。

(2)已知:N2(g)+ O2(g)=2 NO(g) △H=+180 kJ • mol-1
2NO(g)+2 CO(g)=N2(g) + 2 CO2(g) △H=-746 kJ • mol-1
则反应CO(g) + O2(g)=CO2(g)的 △H= kJ • mol-1。
O2(g)=CO2(g)的 △H= kJ • mol-1。
(3)在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 。
2NH3(g) △H <0, 若第5分钟时达到平衡,此时测得NH3的物质的量为0.2 mol,平衡时H2的转化率为 。
(4) 在固定体积的密闭容器中,1.0×103 kPa时,发生反应 N2(g)+3H2(g) 2NH3(g) △H<0,
2NH3(g) △H<0,
其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 51 | K1 | K2 |
① K1 K2(填写“>”、“=”或“<”)
②下列各项能说明上述合成氨反应一定达到平衡状态的是 (填字母)。
a.容器内N2、H2、NH3的浓度之比为1:3:2 b.NH3的浓度保持不变
c.容器内压强保持不变 d.混合气体的密度保持不变
从下列实验事实所引出的相应结论正确的是
| 选项 | 实 验 事 实 | 结 论 |
| A | 其他条件相同,硫代硫酸钠溶液浓度越大,析出硫沉淀所需时间越短 | 当其他条件不变时,增大反应物浓度化学反应速率加快 |
| B | 在化学反应前后,催化剂的质量和化学性质都没有发生改变 | 催化剂一定不参与化学反应 |
| C | 等体积H+浓度相同的盐酸和醋酸同时分别与少量等质量的形状相同的锌粒反应 | 产生氢气的质量相同 |
| D | 在容积可变的密闭容器中发生反应: H2(g)+I2(g) | 正反应速率加快,逆反应速率不变 |
 2HI(g),把容积缩小一倍
2HI(g),把容积缩小一倍 2C(g) △H﹥0,下列图象中正确的是
2C(g) △H﹥0,下列图象中正确的是
