某学生为测定某氨水中NH3∙H2O的物质的量浓度,进行如下实验(已知硫酸铵溶液呈弱酸性):
I.将浓度为0.1000 mol·L-1的标准硫酸溶液装入洗涤、润洗后的酸式滴定管中,调节液面,记录读数;
II.用碱式滴定管移取20.00 mL待测液于锥形瓶中,并滴几滴甲基橙指示剂;
III.在锥形瓶下垫一张白纸,滴定,记录读数。
IV.再重复上述操作两次。
试填空:
(1)装入标准溶液后,调节液面之前应进行的操作是 ;
(2) III步操作中的锥形瓶下垫一张白纸的作用是 ;
(3)滴定过程发生反应的离子方程式为: ,判断滴定终点依据的实验现象是 ;
(4)硫酸溶液读数如下表所示,按所得数据可得氨水中NH3∙H2O的物质的量浓度为__________。
| 滴定前 | 滴定后 | |
| 第一次 | 0.70 | 16.15 |
| 第二次 | 0.05 | 16.35 |
| 第三次 | 0.35 | 15.70 |
(5)下列操作中会使所测NH3∙H2O的物质的量浓度偏低的是__________。
a.I步操作中未用标准酸溶液润洗滴定管
b.I步操作中改用酚酞试液做酸碱指示剂
c.II步操作中用待测液润洗锥形瓶
d.III步操作后发现滴定管尖嘴部有气泡且未处理
e.读取硫酸体积时,开始时仰视读数,结束时俯视读数
 N2O4
N2O4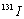 和
和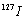 是互为同位素,化学性质几乎相同
是互为同位素,化学性质几乎相同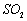 ,造成大气污染,从而使雨水的
,造成大气污染,从而使雨水的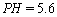 ,形成酸雨
,形成酸雨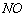 和
和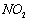 等氮氧化物是形成光化学烟雾和酸雨的一个重要原因
等氮氧化物是形成光化学烟雾和酸雨的一个重要原因

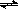 CO(g)+3H2(g) ΔH=QkJ/mol (Ⅰ)
CO(g)+3H2(g) ΔH=QkJ/mol (Ⅰ)