下列说法正确的是( )
| A、CH3CH2CH2CH3的二氯取代产物只有5种结构 |
| B、油脂的种类很多,但它们水解后都有一相同产物 |
| C、乙烯、苯、纤维素均属于烃类化合物 |
| D、苯和乙烯都能使溴水层褪色,均与溴水发生加成反应 |
下列说法中正确的是( )
| A、NO2溶于水得到HNO3,所以NO2属于酸性氧化物 |
| B、过氧化钠与水反应的离子方程式为:Na2O2+2H2O═2Na++2OH-+O2↑ |
| C、漂白粉和水玻璃长期暴露在空气中失效,其原理完全相同 |
| D、足量Zn与一定量浓硫酸充分反应得到混合气体 |
下列排列顺序不正确的是( )
| A、酸性:H3AsO4>H2SO4>H3PO4 |
| B、微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C、热稳定性:HF>HCl>HBr>HI |
| D、熔点:SiO2>NaCl>I2 |
下列说法正确的是( )
| A、SO2通入品红溶液,溶液褪色的原理与SO2通入溴水后褪色的原理相同 |
| B、浓硫酸具有强氧化性,稀硫酸不具有氧化性 |
| C、用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体 |
| D、明矾和漂白粉常用于自来水的净化和杀菌消毒,但二者的作用原理不同 |
下列说法正确的是( )
| A、在300℃、70MPa下由二氧化碳和氢气合成乙醇已成为现实.2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g),则可推测该反应是吸热反应 | ||
B、室温下,将浓度为0.1mol?L?1HF溶液加水稀释,其电离平衡常数和
| ||
| C、电解精练铜时,阳极泥中常含有金属金、银、锌等 | ||
| D、锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除 |
下列有关物质性质的应用正确的是( )
| A、P2O5能与水反应,可用于干燥氨气 |
| B、MgO是一种电解质,工业上常用电解MgO冶镁 |
| C、福尔马林具有防腐杀菌效果,可用于浸制生物标本 |
| D、PbO2具有氧化性和导电性,可用作铅蓄电池负极材料 |
下列反应的离子方程式不正确的是( )
| A、将CO2通入到纯碱饱和溶液中:2Na++CO32-+CO2+H2O═2NaHCO3↓ | ||||
| B、在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入稀盐酸:3Fe2++4H++NO3-═3Fe3++NO↑+2H2O | ||||
| C、向Ba(OH)2溶液中加入足量的NH4HCO3溶液:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O | ||||
D、将饱和FeCl3溶液滴入沸水中制胶体:Fe3++3H2O
|
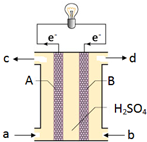 “长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )
“长征”火箭发射使用的燃料是偏二甲肼(C2H8N2),并使用四氧化二氮作为氧化剂,这种组合的两大优点是,既能在短时间内产生巨大能量将火箭送上太空,产物又不污染空气(产物都是空气成分).某校外研究性学习小组拟将此原理设计为原电池,如图所示,结合学习过的电化学原理分析其设计方案,下列说法正确的是( )| A、B为正极 |
| B、从a口通入四氧化二氮气体 |
| C、从d口排除的是NO气体 |
| D、A极发生的电极反应式:C2H8N2-16e-+8H2O=CO2+N2+16H+ |
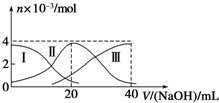 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)所示.根据图示判断,下列说法正确的是( )| A、当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) |
| B、等浓度的NaOH溶液与H2A溶液按2:1混合后,其溶液中水的电离程度比纯水大 |
| C、NaHA溶液中:c(OH-)=c(H+)+c(HA-)+2c(H2A) |
| D、向上述加入20mL NaOH溶液后所得溶液中再加入水的过程中,pH可能减少 |