0 136113 136121 136127 136131 136137 136139 136143 136149 136151 136157 136163 136167 136169 136173 136179 136181 136187 136191 136193 136197 136199 136203 136205 136207 136208 136209 136211 136212 136213 136215 136217 136221 136223 136227 136229 136233 136239 136241 136247 136251 136253 136257 136263 136269 136271 136277 136281 136283 136289 136293 136299 136307 203614
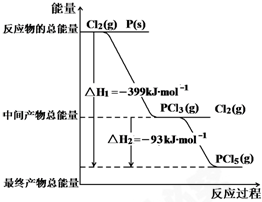 红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题:
红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示( 图中的△H表示生成1mol产物的数据).根据图示,回答下列问题: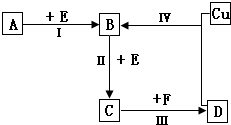 有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题: 某化学研究性学习小组设计制取氯气及探究其性质的方案,并按图所示装置完成实验.(A中发生反应的化学方程式为:MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O)
某化学研究性学习小组设计制取氯气及探究其性质的方案,并按图所示装置完成实验.(A中发生反应的化学方程式为:MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O)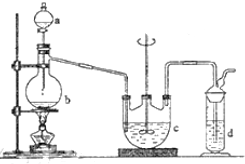 硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示.回答下列问题:
硫代硫酸钠(Na2S2O3)可用做分析试剂及鞣革还原剂.它受热、遇酸易分解.工业上可用反应:2Na2S+Na2CO3+4SO2═3Na2S2O3+CO2制得.实验室模拟该工业过程的装置如图所示.回答下列问题: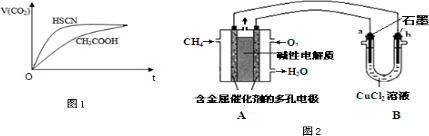
 利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池.已知:
利用太阳能分解水产生H2,在催化剂作用下H2与CO2反应合成CH3OH,并开发出直接以甲醇为燃料的燃料电池.已知: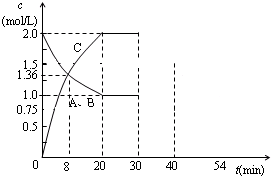 Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应:
Ⅰ、某容积不变的密闭容器中充入等物质的量的气体A和B,某温度下发生反应: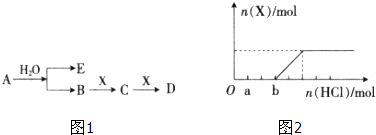
 某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示: