0 136056 136064 136070 136074 136080 136082 136086 136092 136094 136100 136106 136110 136112 136116 136122 136124 136130 136134 136136 136140 136142 136146 136148 136150 136151 136152 136154 136155 136156 136158 136160 136164 136166 136170 136172 136176 136182 136184 136190 136194 136196 136200 136206 136212 136214 136220 136224 136226 136232 136236 136242 136250 203614



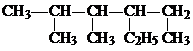 的名称是
的名称是 化合物A中含氧官能团的名称
化合物A中含氧官能团的名称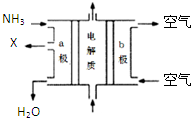 工业废水中含有多种有害成分,任意排放将造成严重污染,进行分类处理达标后才能排放.
工业废水中含有多种有害成分,任意排放将造成严重污染,进行分类处理达标后才能排放.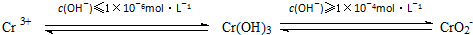
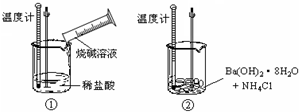
 某校化学实验小组同学进行有关NO2气体的系列实验.
某校化学实验小组同学进行有关NO2气体的系列实验.
 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.