在同温同压下,相同质量的下列气体中所含气体体积最大的是( )
| A、Cl2 |
| B、CO2 |
| C、CH4 |
| D、O2 |
下列变化中,需要加入氧化剂才能实现的是( )
| A、HCl→H2 |
| B、FeO→Fe2+ |
| C、SO2→SO3 |
| D、CO32-→CO2 |
下列叙述正确的是( )
| A、将40g NaOH溶解于1L水中,得到1mol?L-1的NaOH溶液 |
| B、将11.2L HCl气体通入水中配成0.5L溶液,浓度为1mol?L-1 |
| C、将1L 10 mol?L-1的盐酸与9L水混合,混合液浓度为1mol?L-1 |
| D、10g NaOH溶解在水中配成250mL溶液,其浓度为1mol?L-1 |
下列解释事实的方程式不准确的是( )
| A、绿矾久存,表面变黄褐色:4(FeSO4?7H2O)+O2=4Fe(OH)SO4+26H2O |
| B、不能用玻璃塞试剂瓶盛放强碱性溶液:SiO2+2OH-=SiO32-+H2O |
| C、淡黄色的过氧化钠粉末久存,表面变白:2Na2O2=2Na2O+O2 |
| D、长期盛放石灰水的试剂瓶内壁出现白色固体:Ca(OH)2+CO2=CaCO3↓+H2O |
下列表述不正确的是( )
| A、常温下pH为5的盐酸溶液稀释1000倍后,pH等于8 |
| B、NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中阴离子只有CO32-和OH- |
| D、常温下,pH=7的CH3COOH与CH3COONa混合溶液中,c(Na+)=c(CH3COO-) |
下列说法正确的是( )
| A、CS2为V形的极性分子 |
| B、电子云示意图中的每个小黑点都表示一个电子 |
| C、非极性键也可以存在于化合物中 |
| D、甲烷、氨和水都是由极性键结合而成的极性分子 |
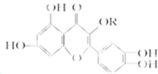 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、可以和溴水反应 |
| B、可用有机溶剂萃取 |
| C、1mol 维生素P可以和7mol H2反应 |
| D、1mol 维生素P可以和4mol NaOH反应 |
下列各组离子在水溶液中不能发生反应的是( )
| A、Ag+、Cl- |
| B、H+、OH- |
| C、Na+、Cl- |
| D、Ba2+、SO42- |
下列结论错误的是( )
①微粒半径:K+>Al3+>S2->C1-
②氢化物的稳定性:HF>HC1>H2S>PH3>SiH4
③离子的还原性:S2->C1->Br->I-
④氧化性:C12>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>S2->C1-
②氢化物的稳定性:HF>HC1>H2S>PH3>SiH4
③离子的还原性:S2->C1->Br->I-
④氧化性:C12>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A、只有① | B、①③ |
| C、②④⑤ | D、①③⑤ |
海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示.下列说法错误的是( )


| A、试剂1可以选用石灰乳 |
| B、从苦卤中提取Br2的反应的离子方程式为:2Br-+Cl2═2Cl-+Br2 |
| C、工业上,电解熔融MgO冶炼金属镁可减小能耗 |
| D、可用BaCl2溶液除去粗盐中的SO42- |