钴在自然界中只存在一种稳定的同位素Co-59,而Co-60是一种穿透力很强的核辐射元素,可用来治疗癌症.下列说法正确的是( )
| A、 27 59Co 原子核内含有59个质子 |
| B、Co-59和Co-60互为同位素 |
| C、 27 60Co 原子核内含有43个中子 |
| D、 27 60Co 原子的最外层电子数为27 |
X、Y是元素周期表中的两种元素.下列叙述中能说明X的非金属性比Y强的是( )
| A、X的气态氢化物比Y的气态氢化物稳定 |
| B、X氢化物水溶液的酸性比Y的氢化物水溶液的酸性强 |
| C、达8电子结构时X原子得到电子数比Y多 |
| D、Y的单质能将X从NaX 的溶液中置换出来 |
下列说法正确的是( )
| A、液态氯化氢是电解质 |
| B、氢氧化铁胶体带正电 |
| C、强电解质溶液导电能力一定强 |
| D、催化剂不参加化学反应 |
设NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A、常温常压下,23克的NO2含有氧原子数为NA |
| B、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| C、含NA个氧原子的O2与含NA个氧原子的O3的质量之比为3:2 |
| D、常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.2NA |
下列各组中的两种物质相互作用时,反应条件或反应物的用量改变,对生成物没有影响的是( )
| A、过氧化钠和二氧化碳 |
| B、钠和氧气 |
| C、氢氧化钠和二氧化碳 |
| D、碳和氧气 |
高温电解石灰石生产CaO的工作原理如图.下列说法不正确的是( )


| A、CO32-向阳极移动 |
| B、阴极电极反应式为3CO2+4e-═C+2CO32- |
| C、该装置可实现太阳能直接转化为化学能 |
| D、该装置可实现CO2零排放 |
除去下列物质中所含的杂质(括号内为杂质),选用试剂正确的是( )
| A、Al2O3(SiO2):NaOH溶液 |
| B、CO2(SO2):Na2CO3溶液 |
| C、FeCl2溶液(FeCl3):Fe粉 |
| D、NaHCO3溶液(Na2CO3溶液):Ca(OH)2溶液 |
下列反应的离子方程式正确的是( )
| A、向澄清石灰水中加入过量的二氧化碳:Ca2++2CO2+2OH-═Ca(HCO3)2 | ||||
B、在硫酸铁溶液中加入足量氢氧化钡溶液:Ba2++SO
| ||||
C、用足量氢氧化钠溶液吸收二氧化碳:2OH-+CO2═CO
| ||||
D、碳酸钠溶液与硫酸溶液反应:CO
|
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KmnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
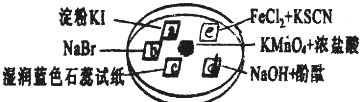
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )

已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )
| A、a、b两处均有颜色变化,证明单质氧化性:CI2>Br2>I2 |
| B、c处先变红,后褪色,证明氯气与水反应生成了酸性物质 |
| C、d处立即褪色,证明氯气与水反应生成了漂白性物质 |
| D、e处变红色,证明氧化性:C12>Fe3+,还原性:Cl-<Fe2+ |