下列叙述中正确的是( )
| A、元素电负性越大,元素第一电离能越大 |
| B、键能越大,键长越长,共价化合物越稳定 |
| C、副族元素中没有非金属元素 |
| D、离子化合物的熔点一定比共价化合物的高 |
下列离子方程式正确的是( )
| A、石灰水与过量碳酸氢钠溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| B、硫酸氢钠溶液中加入氢氧化钡溶液至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| C、氧化铜与稀硫酸反应:2H++O2-=H2O |
| D、碳酸氢钠溶液中加入盐酸:CO32-+2H+=CO2↑+H2O |
NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标况下,2.24L乙醇含有0.2NA个碳原子 | ||
B、CO2通过Na2O2使其增重a g时,反应中转移的电子数为
| ||
| C、3.0gNO与1.12LO2(标况下)反应后,气体分子数可能为0.06NA | ||
| D、200mL2mol/L的NaOH溶液中,含有0.4NA个共价键 |
下列关于0.1mol/L NaHCO3溶液的说法中正确的是( )
| A、常温下pH<7 |
| B、c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) |
| C、c(CO32-)+c(HCO3-)+c(H2CO3)=c(Na+) |
| D、c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
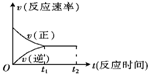 一定条件下的某可逆反应中,正、逆反应速率[用v(正)、v(逆)表示]随时间变化如图所示,则下列说法中错误的是( )
一定条件下的某可逆反应中,正、逆反应速率[用v(正)、v(逆)表示]随时间变化如图所示,则下列说法中错误的是( )| A、在O~t1间,v(正)>v(逆) |
| B、在t1~t2间,v(正)=v(逆) |
| C、在t1时刻,反应在给定的条件下达到了最大限度 |
| D、在t1以后,平衡状态不受任何因素的影响 |
储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-═Cu↓+H2↑+2H2O+2HCOO-,下列说法错误的是( )
| A、电镀过程中氢气在镀件表面析出 |
| B、电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应 |
| C、阳极反应式为HCHO+3OH--2e-=2H2O+HCOO- |
| D、电镀时每生成6.4g铜镀层放出2.24L H2 |
下列物质中,能够导电的电解质是( )
| A、稀硫酸溶液 |
| B、固体KCl |
| C、铜导线 |
| D、熔融的 NaCl |
下列说法正确的是( )
| A、化合反应一定是放热反应 |
| B、分解反应一定是吸热反应 |
| C、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| D、破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为放热反应 |
下列说法正确的是( )
| A、离子化合物中可能含有共价键,但不一定含有金属元素 |
| B、分子中一定含有共价键 |
| C、非极性分子中一定存在非极性键 |
| D、对于组成结构相似的分子,一定是相对分子质量越大,熔沸点越高 |




