0 136018 136026 136032 136036 136042 136044 136048 136054 136056 136062 136068 136072 136074 136078 136084 136086 136092 136096 136098 136102 136104 136108 136110 136112 136113 136114 136116 136117 136118 136120 136122 136126 136128 136132 136134 136138 136144 136146 136152 136156 136158 136162 136168 136174 136176 136182 136186 136188 136194 136198 136204 136212 203614
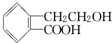 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.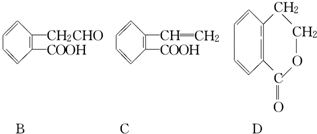

 i.
i. j.
j. k.
k.