下列有关实验操作的叙述中,正确的是( )


| A、可用右图所示的方法将烧杯中的溶液转移到容量瓶中 |
| B、容量瓶可用于配制溶液,但不能作为反应容器使用 |
| C、稀释浓硫酸时,先向烧杯中注入浓硫酸,再加水稀释 |
| D、用托盘天平称量NaOH固体时,需将NaOH固体放在托盘上的纸上 |
工业上常用还原沉淀法处理含铬废水(Cr2O72-和CrO42-),其流程为:
已知:CrO
Cr2O
Cr3+
Cr(OH)3↓
(1)步骤①中存在平衡:2CrO42-(黄色)+2H+?Cr2O42-(橙色)+H2O
(2)步骤③生成的Cr(OH)3,在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5mol?L-1 时可视作该离子不存下列有关说法中,正确的是( )
已知:CrO
2- 4 |
| H+ |
| ①转化 |
2- 7 |
| Fe2+ |
| ②还原 |
| OH- |
| ③沉淀 |
(1)步骤①中存在平衡:2CrO42-(黄色)+2H+?Cr2O42-(橙色)+H2O
(2)步骤③生成的Cr(OH)3,在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)?Cr3+(aq)+3OH-(aq)
(3)常温下,Cr(OH)3的溶度积Ksp=10-32;且当溶液中离子浓度小于10-5mol?L-1 时可视作该离子不存下列有关说法中,正确的是( )
| A、步骤①中加酸,将溶液的pH 调节至2,溶液显黄色,CrO42-离子浓度增大 |
| B、步骤①中当2v(CrO42-)=v(Cr2O72-)时,说明反应2CrO42-(黄色)+2H+?Cr2O72-(橙色)+H2O达到平衡状态 |
| C、步骤②中,若要还原1mol Cr2O72-离子,需要12mol (NH4)2Fe(SO4)2?6H2O |
| D、步骤③中,当将溶液的pH调节至6 时,则可认为废水中的铬已除尽 |
下列有关一些实验仪器用途,说法正确的是( )
| A、食盐水放在试管中进行蒸发可得到NaCl固体 |
| B、过滤操作中,使用玻璃仪器有烧杯、漏斗、玻璃棒 |
| C、分液漏斗能用于混合物混合物的分离和组装滴加液体制气体的发生装置 |
| D、可用量筒快速配制一定体积、一定物质的量浓度的溶液 |
氧化还原反应在生产生活中具有广泛的用途.下列事实不涉及氧化还原反应的是( )
| A、食物腐败 |
| B、点制豆腐 |
| C、金属锈蚀 |
| D、久置氢氧化钠会变质 |
下列各组微粒中,互为同位素的是( )
| A、40Ca和40Ar |
| B、H2O和H2O2 |
| C、O2和O3 |
| D、H、D、T |
由乙烯(CH2=CH2)推测丙烯(CH2=CH-CH3)的结构或性质,正确的是( )
| A、能使酸性KMnO4溶液退色,且丙烯发生加成反应 |
| B、不能使溴的四氯化碳溶液退色 |
| C、丙烯分子中最多可能有7个原子共面 |
| D、与HCl在一定条件下加成只得到一种产物 |
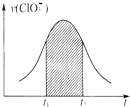 氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应V-t图.下列说法中不正确的是( )
氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平).已知该反应的速率随c(H+)的增大而加快.下列为用ClO3-在单位时间内物质的量浓度变化表示的该反应V-t图.下列说法中不正确的是( )| A、反应开始时速率增大可能是c(H+)所致 |
| B、纵座标为V(H+)的V-t曲线与图中曲线完全重合 |
| C、后期反应速率下降的主要原因是反应物浓度减小 |
| D、图中阴影部分“面积”可以表示t1-t2时间为n(Cl-)增加 |
下列物质中,只能在水溶液中导电的电解质是( )
| A、CO2 |
| B、H2SO4 |
| C、Cl2 |
| D、NaCl |
 按右图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电-段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).则下列叙述中正确的是( )
按右图装置实验,A、B两烧杯分别盛放200g 10%NaOH和足量CuSO4溶液.通电-段时间后,c极上有Cu析出;又测得A杯中溶液的质量减少4.5g (不考虑水的蒸发).则下列叙述中正确的是( )| A、电源P极为负极 |
| B、标准状况下,b极产生气体的体积为5.6 L |
| C、c极上析出固体的质量为32 g |
| D、a极上所发生的电极反应式为40H--4e-=2H2O+O2↑ |
下列物理变化过程中,化学键被破坏的是( )
| A、碘升华 |
| B、冰融化成水 |
| C、蔗糖溶于水 |
| D、氯化钠晶体在熔化状态下电离 |