下列反应的离子方程式,书写错误的是( )
| A、氢氧化钠与盐酸反应 OH-+H+═H2O |
| B、用稀硫酸清除铁锈 Fe2O3+6H+═2Fe3++3H2O |
| C、食盐水中滴加硝酸银溶液 Cl-+Ag+═AgCl↓ |
| D、氢氧化钡跟硫酸铜溶液反应 Ba2++SO42-═BaSO4↓ |
下列关于含Na元素、C1元素的物质的性质叙述正确的是( )
| A、Na单质在空气中缓慢氧化与燃烧的产物都是Na2O2 |
| B、Na2O与Na2O2都能与水反应,产物相同 |
| C、C12与H2混合光照爆炸,H2在C12也能平静的燃烧 |
| D、C12能与NaOH溶液反应,S单质与NaOH溶液加热也不反应 |
| E、C12能与NaOH溶液反应,S单质与NaOH溶液加热也不反应 |
地壳中含量最多的元素是( )
| A、铝 | B、铁 | C、氧 | D、硅 |
下列说法正确的是( )
| A、两种难溶物中溶解度小的物质其KSP不一定小 |
| B、同种酸形成的酸式盐溶解度一定比正盐的溶解度大 |
| C、因为Ksp(BaSO4)=1.08×l0-10,Ksp(BaCO3)=8.1×10-9,所以BaSO4沉淀不可能转化为BaCO3沉淀 |
| D、相同温度下,将足量AgCl固体分别加入同体积的①0.1mo1?L-1盐酸、②0.1mo1?L-1氯化镁溶液、③0.1mo1?L-1硝酸银溶液中,c(Ag+):③>②>① |
下列各组离子在水溶液中可以大量共存的是( )
A、H+、Na+、NO
| ||
| B、SO42-、H+、Ba2+、Cl- | ||
| C、NH4+、K+、OH-、I- | ||
D、H+、Fe2+、NO
|
实验室需要用960mL0.1mol?L-1的Na2CO3溶液,现选用1000mL容量瓶进行配制,以下操作使配得溶液浓度偏低的是( )
| A、称取10.2g Na2CO3,配成1000mL溶液 |
| B、称取10.6g Na2CO3,配成1000mL溶液 |
| C、称量固体时,天平指针偏右 |
| D、定容时俯视液面 |
下列各组物质全部是弱电解质的是( )
| A、H2SiO3 H2S CO2 |
| B、MgSO4 CH3COOH CH3CH2OH |
| C、H2SO3 BaSO4 CH4 |
| D、H2O NH3?H2O H3PO4 |
标准状态下,气态分子断开1mol化学键的焓变为键焓.已知H-H,H-O和O=O键的键焓△H分别为436kJ?mol-1、463kJ?mol-1和495kJ?mol-1.下列热化学方程式正确的是( )
A、H2O(g)═H2(g)+
| ||
B、H2O(g)═H2(g)+
| ||
| C、2H2(g)+O2(g)═2H2O(g)△H=+485kJ?mol-1 | ||
| D、2H2(g)+O2(g)═2H2O(g)△H=-485kJ?mol-1 |
与F-所含质子数与电子数均相等的微粒是( )
| A、OH- |
| B、NH3 |
| C、O2- |
| D、H3O+ |
下列关于价电子排布为3s23p4的粒子描述正确的是( )
| A、该元素在周期表中的位置为第三周期第IVA族 |
| B、该元素的最高正价为+6价 |
| C、一定条件下,它可与H2生成液态化合物 |
D、其核外电子排布图为: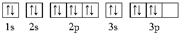 |