下列各组中两种物质在溶液里的反应,可用同一离子方程式表示的是( )
| A、KCl+AgNO3;AlCl3+AgNO3 |
| B、NaHCO3+H2SO4;Na2CO3+HCl |
| C、NaHCO3+NaOH;KHCO3+KOH |
| D、BaCl2+H2SO4;Ba(OH)2+H2SO4 |
下列反应中,水作为氧化剂的是( )
| A、Cl2+H2O═HCl+HClO |
| B、2F2+H2O═4HF+O2 |
| C、2Na+2H2O═2 NaOH+H2↑ |
| D、SO3+H2O═H2SO4 |
从矿物学资料查得,一定条件下自然界存在如下反应14CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4.下列说法正确的是( )
| A、FeS2只作氧化剂 |
| B、被氧化的硫元素和被还原的硫元素的质量比为3:7 |
| C、生成7 mol Cu2S,有10 mol电子转移 |
| D、氧化剂与还原剂物质的量之比为14:5 |
某浓度的铬酸溶液(H2CrO4),向其中加入少量碱以调节pH值(忽略溶液体积变化),下表为各离子浓度(mol/L)与pH之间的关系如下表,下列说法不正确的是( )
| pH | [H2CrO4] | [HCrO4-] | [CrO42-] | [Cr2O72-] |
| 4 | 0 | 0.095 | 0.035 | 0.435 |
| 7 | 0 | 0.086 | 0.274 | 0.320 |
| 10 | 0 | 0.004 | 0.990 | 0.003 |
| A、铬酸的电离方程式为H2CrO4═2H++CrO42- |
| B、铬酸的总浓度为1mol/L |
| C、[H+]越大,HCrO4-浓度越大 |
| D、已知Cr2O72-为橙色离子,CrO42-为黄色离子,随着pH的升高溶液将逐渐变为黄色 |
若NA代表阿伏加德罗常数,下列说法正确的是( )
| A、2.4g金属镁全部变成镁离子时失去的电子数目为0.1NA |
| B、1.0 mol任何单质气体的分子数均为NA,原子数均为2NA,体积均为22.4L |
| C、17gNH3 所含的原子数目为4NA |
| D、0.5mol/L Na2SO4溶液中含有Na+的数目为NA |
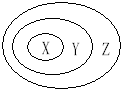 下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )
下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )| A、置换反应、氧化还原反应、化学反应 |
| B、胶体、溶液、混合物 |
| C、NaOH、电解质、化合物 |
| D、Fe2O3、金属氧化物、氧化物 |
铜锌原电池(如图)工作时,下列叙述正确的是( )
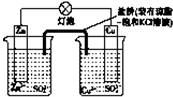

| A、负极反应为 Zn+2e-=Zn2+ |
| B、盐桥中的K+移向ZnSO4溶液 |
| C、在外电路中,电流从负极流向正极 |
| D、电池反应为 Zn+Cu2+═Zn2++Cu |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体质量最大的是( )
| A、20mL2mol/LFeCl3溶液 |
| B、40mL1mol/LNaHCO3溶液 |
| C、20mL1mol/LNa2SO3溶液 |
| D、40mL2mol/LNH4HCO3溶液 |
在溴化钾和碘化钾的混合溶液中通入过量氯气,把溶液蒸干后并将剩余物灼烧,最后残余的物质是( )
| A、氯化钾 |
| B、氯化钾和碘 |
| C、氯化钾和溴 |
| D、氯化钾和溴化钾 |