下列溶液中微粒浓度关系一定正确的是( )
| A、pH=1的一元酸和pH=13的一元碱等体积混合:c(OH-)=c(H+) |
| B、0.1mol/L的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| C、0.1mol/L的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| D、室温下,氢氧化钠与氯化铵的混合溶液中pH=7,则有c(Cl-)=c(NH4+)+c(Na+) |
下列说法正确的是( )
| A、乙酸乙酯和纤维素乙酸酯均可水解生成乙醇 |
| B、溴乙烷、苯酚一定条件下都能与NaOH水溶液发生反应 |
| C、苯、乙烯都能使酸性KMnO4溶液褪色 |
| D、葡萄糖和蔗糖溶液都能发生银镜反应 |
已知反应:H2S(g)+aO2(g)═X+cH2O(l)△H,若△H表示H2S燃烧热,则X为( )
| A、S(s) |
| B、SO2(g) |
| C、SO3(g) |
| D、SO3(l) |
某实验小组依据反应AsO43-+2H++2I-?AsO33-+I2+H2O设计如图1原电池,探究pH对AsO43-氧化性的影响.测得电压与pH的关系如图2.下列有关叙述错误的是( )


| A、调节pH可以改变反应的方向 |
| B、pH=0.68时,反应处于平衡状态 |
| C、pH=5时,负极电极反应式为2I--2e-=I2 |
| D、pH>0.68时,氧化性I2>AsO43- |
化石燃料仍是目前能源的主体,但已经面临危机,开发新能源是解决能源问题的关键.下列能量转换过程,不涉及化学变化的是( )
| A、利用氢氧燃料电池提供电能 |
| B、利用太阳能分解水制备氢气 |
| C、利用水流驱动涡轮机发电 |
| D、利用植物秸秆为原料生产乙醇燃料 |
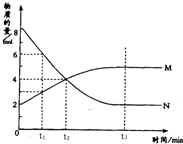 在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N两种气体的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为N=2M |
| B、t1时,N的浓度是M浓度的2倍 |
| C、t2时,正逆反应速率相等达到平衡状态 |
| D、t3时,正逆反应速率相等达到平衡状态 |
下列玻璃仪器中,不能用于加热的有( )
| A、烧杯 | B、容量瓶 |
| C、量筒 | D、试剂瓶 |
我国科学家研制出一种催化剂,它能在室温下高效催化使空气中甲醛被氧化,其反应如下:HCHO+O2
CO2+H2O.下列有关说法正确的是( )
| 催化剂 |
| A、该反应为吸热反应 |
| B、HCHO分子是一种极性分子 |
| C、CO2分子中的化学键为非极性键 |
| D、每生成44g CO2消耗22.4L O2 |
标准状况下,32g CH4所占体积约为( )
| A、44.8L | B、22.4L |
| C、11.2L | D、5.6L |
区别花生油和溶剂油,可用的试剂是( )
| A、水 | B、酚酞试液 |
| C、烧碱溶液 | D、硫酸溶液 |