下列离子方程式的书写正确的是( )
| A、氢氧化铜中加入盐酸 H++OH-=H2O |
| B、铁与盐酸反应 2Fe+6H+=2Fe3++3H2↑ |
| C、大理石与盐酸反应放出CO2气体:CO32-+2H+=CO2+H2O |
| D、氯化铁溶液中加入氢氧化钠溶液Fe3++3OH-=Fe(OH)3↓ |
已知某一微粒的核电荷数,则下列一定可以确定的是其( )
| A、质子数 | B、核外电子数 |
| C、电子层数 | D、最外层电子数 |
下列电离方程式正确的是( )
| A、NH3?H2O═NH4-+OH- |
| B、NaHCO3═Na++H++CO32- |
| C、CH3COONa═CH3COO-+Na+ |
| D、H2S?2H++S2- |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的中子数为9NA |
| B、标准状况下,11.2L苯中含有的碳碳双键数为1.5NA |
| C、42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| D、5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |
NaOH溶液滴定盐酸实验中,不必用到的是( )
| A、酚酞 | B、圆底烧杯 |
| C、锥形瓶 | D、碱式滴定管 |
室温下,对于醋酸及其盐的下列判断正确的是( )
| A、稀醋酸溶解石灰石的离子方程式为CaCO3+2H+═Ca2++H2O+CO2↑ | ||
B、醋酸加水稀释后,溶液中
| ||
C、向稀醋酸中加入等浓度的NaOH溶液,导电能力变化如图 | ||
| D、CH3COONH4溶液和K2SO4溶液均显中性,两溶液中水的电离程度相同 |
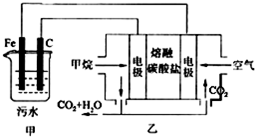 工业上常用Fe做电极电解处理含Cr2O72-的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去.某科研小组用该原理处理污水,设计装置如图所示.下列说法不正确的是( )
工业上常用Fe做电极电解处理含Cr2O72-的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去.某科研小组用该原理处理污水,设计装置如图所示.下列说法不正确的是( )| A、实验时若污水中离子浓度较小,导电能力较差,可加入适量的NaOH |
| B、燃料电池中若有1.6g CH4参加反应,则甲中C电极理论上生成气体体积为8.96L(标准状况下) |
| C、该燃料电池中阴离子移向甲烷一极 |
| D、甲中阳极附近溶液中的离子反应方程式是:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O |
下列离子方程式书写正确的是( )
| A、向碳酸氢钠溶液中加入过量的氢氧化钙溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- |
| B、向NH4HSO4溶液中逐滴滴入Ba(OH)2溶液至恰好沉淀完全2OH-+Ba2++2H++SO42-═2H2O+BaSO4↓ |
| C、向亚硫酸钡固体中加入稀硝酸:3BaSO3+2H++2NO3-═3BaSO4↓+2NO↑+H2O |
| D、石灰乳与碳酸钠溶液混合:Ca2++CO32-═CaCO3↓ |
一定条件将C5H12裂解,最多可以得到烯烃的种数是( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列设备工作时,将化学能转化为热能的是( )
A、 家用燃气灶 |
B、 普通锌锰电池 |
C、 锂离子电池 |
D、 硅太阳能电池 |