反应C(石墨)?C(金刚石)是吸热反应,由此可知( )
| A、金刚石比石墨更稳定 |
| B、等质量的石墨和金刚石,石墨具有的能量比金刚石高 |
| C、石墨比金刚石更稳定 |
| D、金刚石和石墨不能相互转化 |
硝酸生产中,500℃时,NH3和O2可能发生如下反应:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+9072kJ?K=1.1×1026?
②4NH3(g)+4O2(g)?2N2O(g)+6H2O(g)+1105kJ?K=4.4×1028
③4NH3(g)+3O2(g)?2N2(g)+6H2O(g)+1269kJ?K=7.1×1034
其中,②、③是副反应.若要减少副反应,提高NO的产率,最合理的措施是 ( )
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+9072kJ?K=1.1×1026?
②4NH3(g)+4O2(g)?2N2O(g)+6H2O(g)+1105kJ?K=4.4×1028
③4NH3(g)+3O2(g)?2N2(g)+6H2O(g)+1269kJ?K=7.1×1034
其中,②、③是副反应.若要减少副反应,提高NO的产率,最合理的措施是 ( )
| A、减小压强 |
| B、降低温度 |
| C、增大O2浓度 |
| D、使用合适的催化剂 |
下列反应中铁元素被还原的是( )
A、2Fe(OH)3
| ||||
| B、Fe+CuSO4=Cu+FeSO4 | ||||
| C、Fe(OH)3+3HCl=FeCl3+3H2O | ||||
D、2Fe2O3+3C
|
含有非极性键的离子化合物是( )
| A、NaOH |
| B、Na2O2 |
| C、H2O2 |
| D、Cl2 |
25℃时加水稀释10mL pH=11的氨水,下列判断正确的是( )
| A、原氨水的浓度=10-3mol/L | ||||
B、溶液中
| ||||
| C、氨水的电离程度增大,溶液中所有离子的浓度均减小 | ||||
| D、再加入10mL pH=3的盐酸充分反应后混合液的pH值肯定大于7 |
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,由此可判断( )
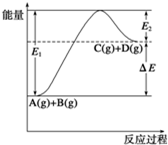

| A、1mol A与1mol B充分反应后,能量变化为△E |
| B、加入催化剂后,反应加快,△E减小 |
| C、反应物的总键能小于生成物的总键能 |
| D、反应达到平衡时,升高温度,A的转化率增大 |
131 55 |
| A、131 | B、76 | C、55 | D、21 |
常温下,0.1mol/L的HA溶液中
=1×10-8,下列叙述中正确的是( )
| c(OH-) |
| c(H+) |
| A、该溶液中由水电离产生的c(H+)=1×10-8mol/L |
| B、0.01mol/LHA的溶液中c(H+)=1×10-4mol/L |
| C、1体积pH=3的HA与10体积pH=11的NaOH混合后溶液中c(OH-)+c(A-)═c(H+)+c(Na+) |
| D、浓度均为0.1 mol/L的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(OH-)-c(H+)<c(HA)-c(A-) |
某元素的原子具有三个电子层,关于其外围电子排布的正确说法是( )
| A、只有s电子 |
| B、只有p电子 |
| C、有s、p电子 |
| D、只有s电子或有s、p电子 |
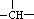 ,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)
,则该结构的烃的一氯取代物最多可能有( )种(不考虑立体异构)