下列离子反应方程式正确的是( )
| A、过量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ |
| B、氨水滴入AlCl3溶液中:Al3++3OH-═Al(OH)3↓ |
| C、FeO溶于稀HCl中:O2-+2H+═H2O |
| D、Al2O3溶于NaOH溶液中:Al2O3+2OH-+3H2O═2[Al(OH)4]- |
用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是( )
| A、有色布条被空气中的氧气氧化 |
| B、漂白粉溶液失去了部分水分,浓度增大了 |
| C、漂白粉和空气中的二氧化碳充分反应生成了次氯酸 |
| D、漂白粉被氧化了 |
短周期元素X、Y、Z的原子序数依次增大,Y为IA族元素,X与Z同主族,3种元素原子的最外层电子数之和为13.下列判断正确的是 ( )
| A、Y元素位于第2周期 |
| B、Y、Z均能与X形成不只一种化合物 |
| C、X是ⅤA族元素 |
| D、氢化物的稳定性:HnZ>HnX |
白磷有毒,不小心粘在皮肤上可用稀硫酸铜溶液冲洗:11P4+60CuSO4+96H2O→20Cu3P+24H3PO4+60H2SO4,被7.5mol硫酸铜氧化的白磷是( )
| A、0.375mol |
| B、0.15mol |
| C、1.375mol |
| D、1.5mol |
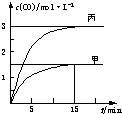 一定条件下存在反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.
一定条件下存在反应:C(s)+H2O(g)?CO(g)+H2(g)△H>0.向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示.| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | V |
| 温度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2mol C、1mol H2O | 1mol CO、1mol H2 | 4mol C、2mol H2O |
| A、甲容器中,反应在前15 min的平均速率v(H2)=0.01 mol?L-1?min-1 |
| B、丙容器的体积V<0.5 L |
| C、当温度为T1℃时,反应的平衡常数K=2.25 |
| D、乙容器中,若平衡时n(H2O)=0.4 mol,则T1<T2 |
海洋中蕴藏着巨大的化学资源.下列有关海水综合利用的说法正确的是( )
| A、蒸发海水可以生产单质碘 |
| B、蒸馏海水可以得到淡水 |
| C、电解海水可以得到单质镁 |
| D、电解海水可以制得金属钠 |
W、X、Y、Z是短周期元素,其部分性质如下表,下列说法正确的是( )
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | Y+与NH4+的质子数、电子数均相等 |
| Z | 第三周期原子半径最小的金属 |
| A、Z的氧化物属于碱性氧化物 |
| B、离子半径:Z>W |
| C、最高价氧化物对应水化物的碱性:Y>Z |
| D、气态氢化物的热稳定性:X>W |
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
| C、化合物YW2、ZW2都是酸性氧化物 |
| D、用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
下列说法不正确的是( )
| A、某烷烃R的相对分子质量为86,1H核磁共振谱(1H-NMR)显示分子中有两个峰.则R的名称一定为2,3一二甲基丁烷 |
B、合成叶蝉散的反应属于加成反应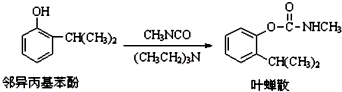 |
| C、有机物CH3(CH2)2CH(CH3)2的一氯代物有四种 |
| D、等质量的乳酸(C3H6O3)和葡萄糖分别完全燃烧,消耗氧气的物质的量相等 |
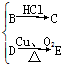 ,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )
,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )