已知4g RO32-中核外电子数比质子数多6.02×1022个,则元素R的相对原子质量为( )
| A、12 | B、27 | C、32 | D、80 |
按下列实验方法能够达到要求的是( )
| A、用10mL量筒量取7.50mL稀盐酸 |
| B、用托盘天平称量出25.20g NaCl晶体 |
| C、用pH试纸测得某碱溶液的pH为12.7 |
| D、用25mL碱式滴定管量出14.08mL NaOH溶液 |
现向一容积不变的2L密闭容器中充入4mol NH3和3mol O2,发生反应4NH3(g)+3O2(g)?2N2(g)+6H2O(g),4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
| A、v(N2)=0.125 mol?L-1?min-1 |
| B、v(H2O)=0.375 mol?L-1?min-1 |
| C、v(O2)=0.225 mol?L-1?min-1 |
| D、v(NH3)=0.250 mol?L-1?min-1 |
下列有关化学用语表示正确的是( )
A、3,3-二甲基-1-戊烯的键线式: |
B、甲醛的电子式: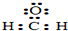 |
C、乙醇分子的比例模型: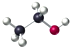 |
D、CH4Si的结构式: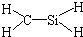 |
 中国人民银行于2011年10月31日发行2012中国壬辰(龙)年金银纪念币一套.该套纪念币共15枚,其中有七枚纪念币外观为银白色,某同学认为其可能是用铁制成的,于是用磁铁来吸引一下,从化学研究方法的角度来看,“用磁铁吸”是研究物质性质的方法中的( )
中国人民银行于2011年10月31日发行2012中国壬辰(龙)年金银纪念币一套.该套纪念币共15枚,其中有七枚纪念币外观为银白色,某同学认为其可能是用铁制成的,于是用磁铁来吸引一下,从化学研究方法的角度来看,“用磁铁吸”是研究物质性质的方法中的( )| A、实验法 | B、观察法 |
| C、假设法 | D、比较法 |
下列叙述不正确的是 ( )
| A、NH3是极性分子,为三角锥形 |
| B、双原子分子中的共价键,一定是非极性键 |
| C、非极性键也可能存在于离子化合物中 |
| D、CO2是非极性分子,分子中C原子处在2个O原子所连成的直线的中央. |
下列选项中所涉及到的两个量的一定相等的是( )
| A、11.2LCl2与4.25gNH3所含有的原子数 |
| B、18.0g重水(D2O)与20gNe所含有的电子数 |
| C、标准状况下36gH2O与1.204×1024个O2分子所占的体积 |
| D、等物质的量的Al分别与足量的盐酸、NaOH溶液反应转移的电子数 |
下列叙述正确的是( )
| A、同种元素的原子均具有相同的质子数和中子数 |
| B、不同元素的原子构成的分子只含极性键 |
| C、第三周期中的非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱 |
| D、第ⅠA族和第ⅦA族元素从上到下随原子序数递增,单质的沸点均逐渐升高 |
下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是( )
| A、V(H2)═0.1mol/(L?min) |
| B、V(N2)═0.1mol/(L?min) |
| C、V(NH3)═0.15mol/(L?min) |
| D、V(N2)═0.002mol/(L?s) |
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴危险警告标签.下面所列物质中,贴错了标签的是
( )
| A | B | C | D | |
| 物质的 化学式 |
H2SO4(浓) | C2H5OH(酒精) | Hg(汞) | NaCl |
| 危险警 告标签 |
 |
 |
 |
 |
| A、A | B、B | C、C | D、D |