0 135768 135776 135782 135786 135792 135794 135798 135804 135806 135812 135818 135822 135824 135828 135834 135836 135842 135846 135848 135852 135854 135858 135860 135862 135863 135864 135866 135867 135868 135870 135872 135876 135878 135882 135884 135888 135894 135896 135902 135906 135908 135912 135918 135924 135926 135932 135936 135938 135944 135948 135954 135962 203614
 在某一容积为5L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:
在某一容积为5L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应: 某研究性学习小组在一次活动中,参照右图组装实验装置,以多孔碳棒为电极,电解质溶液用0.5mol?L-1NaOH溶液,电用3~6V直流电,发光二极管起辉电压为1.7V,电流为0.6mA.(提示:电解NaOH溶液实质上是电解水)
某研究性学习小组在一次活动中,参照右图组装实验装置,以多孔碳棒为电极,电解质溶液用0.5mol?L-1NaOH溶液,电用3~6V直流电,发光二极管起辉电压为1.7V,电流为0.6mA.(提示:电解NaOH溶液实质上是电解水)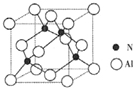 氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
 如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题: 目前正研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
目前正研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:
