设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| B、25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
| C、50mL 18.4mol?L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
| D、常温下,1L 0.1mol?L-1的NH4NO3溶液中氧原子数为0.3NA |
下列说法正确的是( )
| A、离子键只存在于离子化合物中,共价键只存在于共价化合物中 |
| B、热稳定性:NH3>PH3>AsH3;酸性:HClO4>H2SO4>H3PO3 |
| C、BF3和CS2分子中所有原子的最外层都是8电子稳定结构 |
| D、钠离子的半径大于镁离子的半径,氯离子的还原性强于硫离子的还原性 |
下列离子方程式中书写正确的是( )
| A、铝粉与烧碱溶液反应:Al+6OH-═[Al(OH)4]-+H2↑ |
| B、水玻璃中加入稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
| C、二氧化硅与苛性钠溶液反应:SiO2+2OH-═SiO32-+H2O |
| D、在氯化铝溶液中滴加过量的氨水:Al3++4OH-═[Al(OH)4]- |
下列化学用语表示正确的是( )
A、HClO的电子式为 |
B、硝基苯的结构简式为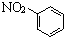 |
| C、饱和醇的通式CnH2n+2O |
D、 表示甲烷分子的球棍模型 表示甲烷分子的球棍模型 |
在四个相同的容器中,在不同的温度下(其它条件相同)进行合成氨的反应,根据下列在相同时间内测得的结果判断,该反应所处的温度最高的是( )
| A、v(NH3)=0.1mol/(L?min) |
| B、v (H2)=0.6mol/(L?min) |
| C、v (N2)=0.3mol/(L?min) |
| D、v (H2)=0.3mol/(L?min) |
下列实验中,能够达到实验目的是( )
A、 实验室制取并收集氨气 |
B、 制取SO2并检验SO2的漂白性 |
C、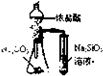 比较氯碳硅三种元素的非金属性强弱 |
D、 除去CO2中的HCl |
下列关于原电池的说法正确的是( )
| A、原电池是将化学能转化为电能的装置 |
| B、构成原电池的正极和负极必须是两种不同的金属 |
| C、原电池放电时,电子由正极流向负极 |
| D、原电池放电时,电流是从负极流向正极 |
用含少量银和锌的粗铜做阳极,纯铜片做阴极,CuSO4溶液做电解液,电解一段时间后,阳极质量减少了x g,则( )
| A、电解液质量增加x g |
| B、阴极质量增加x g |
| C、阴极质量增加a g,a>x |
| D、阴极质量增加b g,b<x |
下列反应中,反应物的总能量一定大于生成物的总能量的是( )
| A、所有氧化还原反应 |
| B、所有不需要加热的反应 |
| C、所有物质的溶解过程 |
| D、所有燃烧反应 |
NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A、0.5molO3与11.2LO2所含的分子数一定相等 |
| B、标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
| C、常温常压下,92g的NO2含有的原子数为6 NA |
| D、1.00mol/L NaCl中,含有Na+的数约为6.02×1023 |