同一周期三种非金属元素X、Y、Z,其最高价氧化物的水化物的酸性由强到弱的顺序是:HXO4>H2YO4>H3ZO4.下列说法正确的是( )
| A、元素的非金属性:X<Y<Z |
| B、气态氢化物的稳定性:HX>H2Y>ZH3 |
| C、阴离子的还原性:X->Y2->Z3- |
| D、X、Y、Z依次位于ⅤA族、ⅥA族、ⅦA族 |
欲除去下列物质中的杂质(括号内物质为杂质),所用试剂不正确的是( )
| A、KNO3溶液(K2SO4):适量Ba(NO3)2溶液 |
| B、CaCO3粉末(CaCl2):过量盐酸 |
| C、Cu粉(Zn粉):过量盐酸 |
| D、CO2(O2):灼热的铜网 |
固体熔化时,必须破坏非极性共价键的是( )
| A、冰 | B、晶体硅 | C、溴 | D、二氧化硅 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、在常温常压下,11.2L N2含有的分子数为0.5NA |
| B、在常温常压下,18 g水中含有的分子数为NA |
| C、含有分子数为NA的氧气的质量是32g/mol |
| D、在2mol/L的MgCl2溶液中含有的Cl-数为4NA |
不能用于判断HA是弱电解质(弱酸)的依据是( )
| A、浓度相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多 |
| B、pH相等的HCl与HA两溶液体积相同时,跟镁反应生成氢气HA比HCl多 |
| C、浓度相等的HCl与HA两溶液,c(H+)HCl约是c(H+)HA的100倍 |
| D、pH相等的HCl与HA两溶液,c(HA)约是c(HCl)的100倍 |
下列反应中Cl2既表现氧化性又表现还原性的反应是( )
| A、Cl2+2NaOH=NaCl+NaClO+H2O |
| B、2HClO═2HCl+O2↑ |
| C、Cl2+2Na═2NaCl |
| D、MnO2+4HCl=MnCl2+Cl2↑+2H2O |
下列物质都能导电,其中属于电解质的是( )
| A、熔融的NaOH | B、金属铝 |
| C、稀硫酸 | D、NaCl溶液 |
S元素最可能是( )
| A、s区元素 | B、稀有气体元素 |
| C、p区元素 | D、d区元素 |
下列说法不正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 |
| C、一定条件下,使用催化剂能加快反应速率 |
| D、相同条件下,溶液中Fe3+、Cu2+、Zn2+的氧化性依次减弱 |
已知断裂1mol C-H键,要吸收热量414.4kJ;断裂1mol C-C键,要吸收热量347.4kJ;生成1mol C═C键,会放出热量615.3kJ;生成1mol H-H键,会放出热量435.3kJ,某有机物分解的反应可表示为: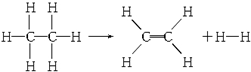
若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )

若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )
| A、该反应放出251.2 kJ的热量 |
| B、该反应吸收251.2 kJ的热量 |
| C、该反应放出125.6 kJ的热量 |
| D、该反应吸收125.6 kJ的热量 |