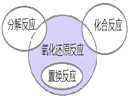
 氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分
氧化还原反应与四种基本反应类型的关系如图所示.下列化学反应属于阴影部分的是( )
| A、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
B、4NH3+5O2
| ||||
| C、2NaHCO3=Na2CO3+H2O+CO2↑ | ||||
| D、Cl2+2NaBr=2NaCl+Br2 |
下列说法中正确的是( )
| A、NH4NO3溶于水吸热,说明其溶于水不是自发过程 |
| B、反应C(s)+CO2(g)═2CO(g)为熵增加的反应,常温下一定自发进行 |
| C、熵增加且放热的反应一定是自发反应 |
| D、非自发反应在任何条件下都不能实现 |
向装有碘水的试管中加CCl4振荡,静置后,你观察到的现象是( )
| A、上层几乎无色,下层紫红色 |
| B、上层紫红色,下层几乎无色 |
| C、上层几乎无色,下层橙色 |
| D、不分层,紫红色 |
已知反应A2(g)+2B2(g)?2AB2(g)△H>0,下列说法正确的是( )
| A、升高温度正反应速率加快,逆反应速率减慢 |
| B、0.1 mol A2和0.2 mol B2反应达到平衡时生成0.2 mol AB2 |
| C、达平衡后,升高温度,B的转化率不变 |
| D、催化剂可同等程度地改变正、逆反应速率 |
下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大
②HCl的酸性比H2S强
③HCl的稳定性比H2S强
④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强
⑥Cl2能与H2S反应生成S
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑧还原性:Cl-<S2-.
①HCl的溶解度比H2S大
②HCl的酸性比H2S强
③HCl的稳定性比H2S强
④HCl的还原性比H2S强
⑤HClO的酸性比H2SO4强
⑥Cl2能与H2S反应生成S
⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS
⑧还原性:Cl-<S2-.
| A、③④⑤⑧ | B、③⑥⑦ |
| C、③⑥⑦⑧ | D、全部 |
下列现象不能用氢键解释的是( )
| A、冰的密度小于液态水 |
| B、NH3容易液化 |
| C、HF的沸点高于HI |
| D、有机物普遍存在同分异构现象 |
某有机物在氧气中充分燃烧,生成水蒸气和CO2的物质的量之比为1:1,由此可以得出的结论是( )
| A、该有机物分子中C、H、O原子个数比为1:2:3 |
| B、分子中C、H原子个数比为1:2 |
| C、有机物中必定含有氧 |
| D、有机物中一定不含氧 |
分离 FeCl3、KCl、CaCO3的固体混合物,应采用的一组试剂是( )
| A、水、硝酸银、稀硝酸 |
| B、水、氢氧化钠、盐酸 |
| C、水、氢氧化钾、盐酸 |
| D、水、氢氧化钾、硫酸 |
下列有关物质的性质和应用的说法均正确的是( )
| A、二氧化硅能与NaOH溶液反应,不能用玻璃瓶盛放NaOH溶液 |
| B、Cl2能与Ca(OH)2反应,可以用澄清石灰水吸收尾气中的Cl2 |
| C、BaCO3、BaSO4都难溶于水,均可用做钡餐 |
| D、Al与Fe2O3能发生铝热反应,可用于焊接钢轨 |
已知1.2g C(石墨)不完全燃烧生成CO,放出11.1kJ热量,继续燃烧又放出28.3kJ热量.则能表示C(石墨)燃烧热的热化学方程式为( )
A、C(石墨 s)+
| ||
B、C(石墨 s)+
| ||
| C、C(石墨 s)+O2(g)=CO2(g)△H=-394kJ?mol-1 | ||
| D、C(石墨 s)+O2(g)=CO2(g)△H=-283kJ?mol-1 |